Атипическая гиперплазия эндометрия
типическая гиперплазия эндометрия — патологическое разрастание внутреннего слоя матки с появлением атипических клеток. Провоцируется избытком эстрогенов и недостатком прогестерона. Рассматривается, как предраковое заболевание. Может развиваться в любом возрасте, однако чаще выявляется после 45 лет. Сопровождается нарушениями менструального цикла и маточными кровотечениями (меноррагиями, метроррагиями). Диагноз устанавливается на основании жалоб, анамнеза и данных дополнительных исследований. Лечение — гормонотерапия, выскабливание или абляция слизистой оболочки.
Симптомы атипической гиперплазии эндометрия
Симптомы атипической гиперплазии эндометрия имеют место в виде тех или иных проявлений присущих каждому конкретному характеру и типу развития патологического процесса. Основным симптомом данного заболевания являются маточные кровотечения. У большинства пациенток такие кровотечения возникают на фоне задержки менструации сроком на 1-3 месяца. Реже (как правило, при отсутствии ожирения и явной эндокринной патологии) наблюдаются регулярные циклы при продолжительности меноррагии более 7 дней. Примерно у четверти больных с атипической гиперплазией эндометрия выявляются ановуляторные маточные кровотечения. В 5-10% случаев диагностируются метроррагии. Возможны скудные кровянистые выделения в середине менструального цикла либо при отсутствии менструаций. Так при железистой форме заболевания, которое по своей сути является доброкачественным, происходит пролиферация стромы и эндометриодных желез. Отмечается утолщение слизистой оболочки, а железы в строме располагаются неправильным образом. Выраженность процессов железистой гиперплазии обуславливает ее дифференциацию на активную, острую стадию заболевания и находящуюся в состоянии покоя, хроническую его форму. Активная форма характеризуется большим количеством клеточных митозов в строме и эпителии желез, что проявляется как следствие продолжительного чрезмерно высокого уровня эстрогенов.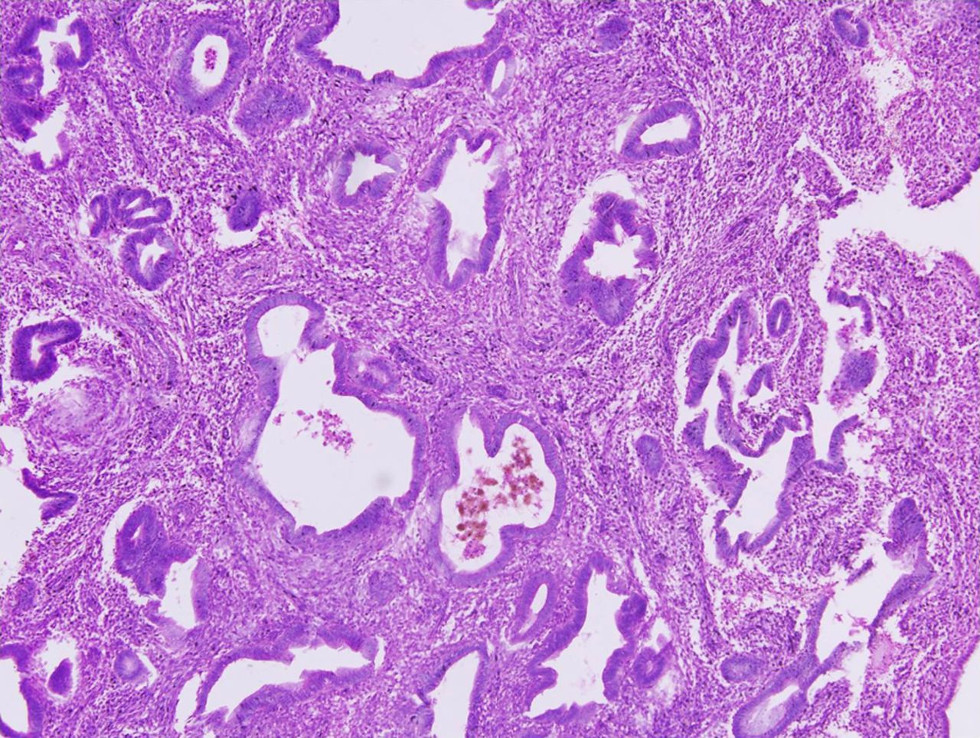
Лечение атипической гиперплазии эндометрия
Лечение данной патологии может быть как консервативным, так и оперативным, проводиться амбулаторно или в условиях стационара. Показанием к плановой госпитализации в репродуктивном возрасте являются кровотечения и кровянистые выделения, в постменопаузе — кровотечения, продолжительные водянистые или гнойные выделения. Экстренная госпитализация показана при обильных кровотечениях. Тактика лечения атипической гиперплазии эндометрия определяется с учетом возраста больной, ее желания иметь детей, наличия соматических заболеваний и болезней репродуктивной системы (особенно — аденомиоза или миомы), формы атипической гиперплазии эндометрия и количества рецидивов. Главным является своевременное выявление этого заболевания или начальных стадий рака, когда атипичные клетки только появились в базальном слое эндометрия. Поэтому все нарушения менструального цикла должны быть немедленно обследованы. Для этого женщинам проводят вначале ультразвуковое исследование матки, а затем, если были выявлены изменения, — эндоскопическое (гистероскопию). Гистероскопия может быть диагностической и лечебной. Чаще всего диагностическая гистероскопия, когда врач глазом рассматривает увеличенный оптической аппаратурой эндометрий, переходит в лечебную, то есть эндометрий удаляется. Но это делается не всегда. В детородном возрасте сегодня стараются использовать в основном гормональную терапию: подавление секреции эстрогенов при помощи препаратов с антиэстрогенными свойствами, прогестагенов (синтетических аналогов прогестерона) или аналогов ризлинг-гормонов гипоталамуса (они подавляют секрецию гормонов гипофиза).
Оперативное лечение гиперплазии эндометрия
Путем выскабливания полости матки врач кюреткой удаляет гиперплазированный эндометрий под визуальным контролем гистероскопа. Полипы удаляют специальными ножницами или щипцами, под контролем зрения их ‘откручивают’ или срезают.Операцию по удалению полипа называют ‘полипэктомией’. Далее после получения результатов гистологического исследования в зависимости от типа гиперплазии, возраста пациентки и сопутствующих заболеваний подбирается гормональная терапия(кроме фиброзных полипов,не требующих гормонального лечения). Цель гормонотерапии — подавить дальнейшую пролиферацию (разрастание) эндометрия и урегулировать гормональный дисбаланс.
Для лечения гиперплазии эндометрия применяются следующие группы гормонов:
— КОК — комбинированные оральные контрацептивы( Регулон, Жанин,Ярина) назначают в течение шести месяцев по контрацептивной схеме. Препараты подходят женщинам репродуктивного возраста до 35 лет, а также девушкам подросткового возраста с обильными и/или нерегулярными менструациями с железистыми и железисто-кистозными типами гиперплазий или полипами.
КОКи можно использовать для ‘гормонального гемостаза'(прием гормонов в больших дозах) у девочек в экстренных ситуациях для остановки кровотечения, чтобы не прибегать к выскабливанию. КОК назначают по 2-3 таблетки в сутки, далее дозу снижают, доводя до 1 таблетки в день. Курс лечения составляет 21 день. При неэффективности гормонального гемостаза — если кровотечение продолжается и угрожает жизни ребенка прибегают к выскабливанию полости матки.
— гестагены (Дюфастон,Утрожестан) с 16 по 25 день менструального цикла назначают на 3-6 месяцев.Подходят женщинам любого возраста с любыми видами гиперплазий. С успехом применяют гестагенсодержащую контрацептивную внутриматочную спираль ‘Мирена’,которая оказывает местный эффект на эндометрий в отличие гестагенов, применяемых оральным путем,которые имеют системное воздействие. Спираль ставят на 5 лет.Минус спирали в том,что довольно часто возникает побочный эффект в виде межменструальных кровяных выделений в течение 3-6 месяцев после постаковки спирали.К тому же многих пациенток смущают мажущий характер менструальных выделений на фоне Мирены и наличие инородного тела в полости матки;
— аГнРГ-агонисты гонадотропин рилизинг-гормона (Золадекс, Бусерелин) -наиболее эффективная группа гормонов. Применяют у женщин после 35 лет и в период перименопаузы от 3 до 6 месяцев при любых формах гиперплазий. Неприятный побочный эффект препаратов данной группы-симптомы раннего климакса (приливы жара). Гонадотропные рилизинг-гормоны образуются в нервных клетках переднего и среднего гипоталамуса и регулируют синтез и выделение гонадотропных гормонов гипофиза, опосредованно — образование половых гормонов в яичниках. Механизм действия агонистов ГнРГ (как и натуральных) состоит в связывании с рецепторами клеток гипофиза, секретирующих гонадотропные гормоны. В результате развивается картина, сходная с наблюдаемой при гипогонадотропной аменорее. Этот феномен называют также ‘медикаментозной кастрацией’. Процесс обратимый: после прекращения введения аГнРГ через 14-21 день восстанавливается функция всей гипоталамо-гипофизарно-яичниковой системы у женщин репродуктивного возраста. Препараты аГнРГ нашли широкое применение в гинекологической клинике, прежде всего при эстрогензависимой патологии: гиперплазии эндометрия, миомах матки, эндометриозе, раке молочных желез. Препараты вводятся раз в 28 дней в течение 3-6 месяцев в зависимости от характера патологического процесса.
Пациентки с атипической гиперплазией эндометрия требуют особого динамического наблюдения гинеколога.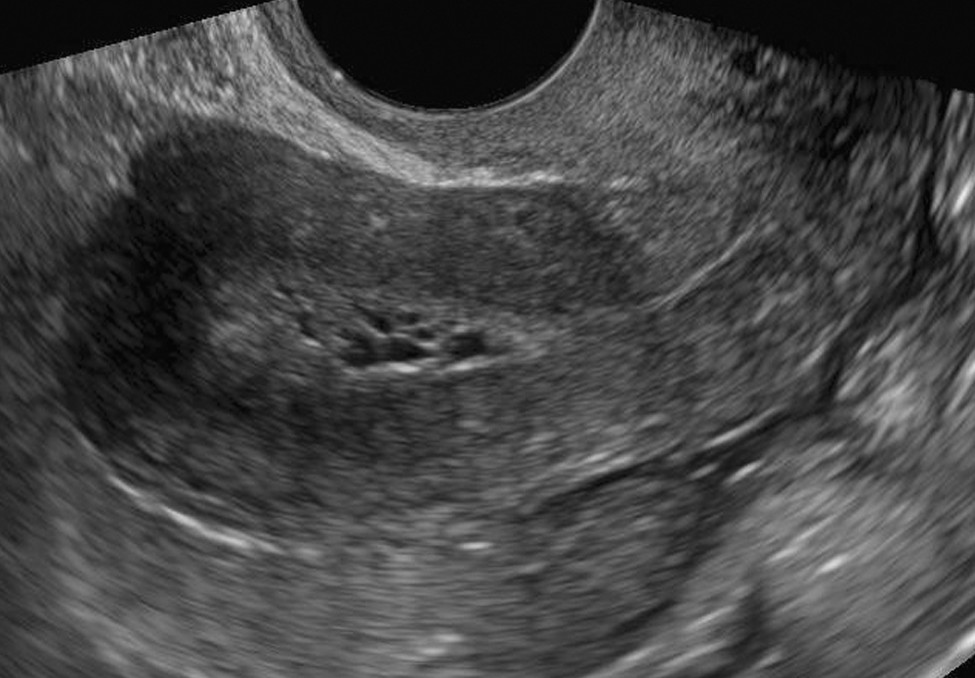 Контрольное УЗИ следует проводить через 3,6 и 12 месяцев после выскабливания и начала приема гормонов для оценки эффективности лечения. При повторном рецидиве аденоматоза показано удаление матки.
Контрольное УЗИ следует проводить через 3,6 и 12 месяцев после выскабливания и начала приема гормонов для оценки эффективности лечения. При повторном рецидиве аденоматоза показано удаление матки.
При рецидиве полипов эндометрия, железистой и железисто-кистозной форм гиперплазий, при неэффективности гормонотерапии — если пациентка не заинтересована в деторождении — показана аблация (резекция) эндометрия — полное разрушение эндометрия. С этой целью применяют электрохирургический (с режущей петлей) и лазерные методы аблации под контролем гистероскопа. Операцию проводят под общим внутривенным наркозом.
После выскабливания полости матки и/или резекции эндометрия пациентка может быть выписана домой в день операции либо на следующий день. В течение 3-10 дней после манипуляции могут быть необильные кровяные выделения из половых путей. После аблации обычно вместе с выделениями выходят остатки резецированных тканей. Подобные выделения являются нормой и не должны смущать. Параллельно с гормонотерапией для быстрого выздоровления показан прием витаминов: аскорбиновая кислота, витамины группы B, препараты железа при анемии ( Сорбифер, Мальтофер). Назначается седативная терапия (настойки валерианы или пустырника). Полезны физиотерапевтические процедуры (электрофорез) и иглорефлексотерапия. Питание должно быть полноценным, необходимо соблюдать режим труда и отдыха. Также рекомендуется половое воздержание в течение 2-х недель после выскабливания.
« На предыдущую страницу
Гиперплазия эндометрия — симптомы и лечение, причины, диагностика, профилактика
Внутренняя оболочка матки у женщины репродуктивного возраста подвержена изменениям под действием половых гормонов – эстрогенов. При их чрезмерной стимуляции возникает гиперплазия эндометрия – его избыточное разрастание, увеличение толщины и изменение клеток. Это состояние является доброкачественным, но в некоторых случаях может привести к раку матки. Заболевание чаще встречается у женщин с нарушениями менструального цикла, а также в постменопаузальном периоде.
Гиперплазия эндометрия: причины и классификация
Основной причиной заболевания является нарушение баланса между двумя половыми гормонами – эстрогеном и прогестероном. Активная эстрогенная стимуляция при недостатке гестагенов приводит к разрастанию клеток эндометрия, как это происходит в первую фазу менструального цикла, но к более выраженному.
Факторы, способные вызвать гормональный дисбаланс:
- синдром поликистозных яичников;
- состояние постменопаузы;
- избыточный вес.
Другие причины гиперплазии эндометрия:
- эндокринные заболевания – диабет, ожирение;
- заболевания яичников;
- прием тамоксифена по поводу рака молочной железы.
В России часто используется такая классификация заболевания:
- эндометриальные полипы;
- простая железистая гиперплазия эндометрия;
- железистокистозная очаговая гиперплазия эндометрия;
- диффузная железистокистозная гиперплазия эндометрия;
- атипическая гиперплазия эндометрия (аденоматоз), очаговая или диффузная, в том числе аденоматозные полипы.
Согласно ВОЗ, различают 2 основных вида этой патологии – без атипии и атипическую. Каждый из них может быть простым и сложным. Клетки, образующие железы эндометрия, претерпевают изменения разной степени выраженности – от незначительных до предраковых. Эта классификация полезна тем, что показывает связь заболевания с развитием злокачественных новообразований.
Эндометрий при железистой гиперплазии разрастается, но его клетки не подвергаются изменениям. Кистозная перестройка – формирование из некоторых желез округлых образований (кист). Это наименее опасная из всех форм заболевания, она хорошо поддается гормональной терапии.
Простая атипичная гиперплазия эндометрия сопровождается изменением свойств клеток на отдельном участке. Она поддается гормональной терапии и имеет низкий риск озлокачествления. Сложная форма этой разновидности патологии – наиболее опасная и часто трансформируется в рак эндометрия. Лечение нередко состоит в удалении матки.
Сложная форма этой разновидности патологии – наиболее опасная и часто трансформируется в рак эндометрия. Лечение нередко состоит в удалении матки.
Гиперплазия эндометрия – симптомы
Наиболее частые признаки гиперплазии эндометрия связаны с изменениями менструального цикла. Они могут наблюдаться ежедневно или в определенные фазы цикла, их выраженность тоже может быть разной.
Основные симптомы гиперплазии эндометрия:
- нерегулярные менструации;
- угревая сыпь на коже;
- сухость во влагалище;
- кровянистые выделения между менструациями;
- боль во время полового акта;
- приливы жара;
- отсутствие менструации;
- учащенное сердцебиение, утомляемость;
- нестабильность настроения;
- усиление роста волос на теле;
- слишком обильные или длительные менструации;
- боль в нижней части живота.
При появлении таких симптомов необходимо обратиться к гинекологу. Специалисты клиники на Барклая, расположенной в Москве, окажут таким пациенткам квалифицированную помощь в диагностике и лечении этого серьезного заболевания.
Диагностика и лечение гиперплазии эндометрия
Главная задача диагностики заболевания – подтвердить утолщение эндометрия и наличие в нем измененных клеток. Это может быть сделано на УЗИ и путем взятия биопсии.
Материал для микроскопического исследования может быть получен в ходе диагностического выскабливания полости матки. Также выполняется аспирационная биопсия – забор материала с помощью зонда, введенного в матку, из которого удаляется воздух и таким образом создается вакуум. Многим пациенткам с этим заболеванием требуется гистероскопия – осмотр внутренней поверхности матки с помощью оптического инструмента; во время процедуры можно взять биопсию или удалить полип.
Для выяснения толщины эндометрия применяется УЗИ. Большей информативностью обладает трансвагинальный метод, когда датчик вводится во влагалище.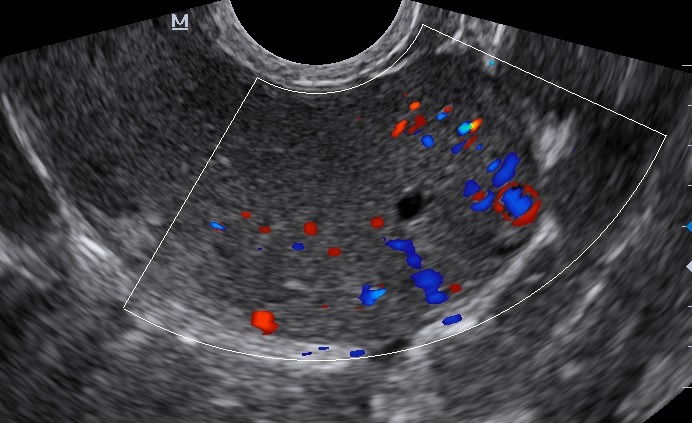 Врач оценивает эхопризнаки заболевания, в том числе и с точки зрения возможного развития рака.
Врач оценивает эхопризнаки заболевания, в том числе и с точки зрения возможного развития рака.
Лечение железистой гиперплазии эндометрия и простой формы атипической гиперплазии проводится с помощью гормональных препаратов. Обычно это средства на основе гестагенов, которые принимают внутрь, или регулярно в форме инъекций, либо путем введения внутриматочной гормональной спирали. Во время такого курса беременность невозможна.
Применяются и другие группы лекарств – антигонадотропные препараты и агонисты гонадотропин-рилизинг гормона.
Также врачи используют кюретаж стенок матки для удаления разросшихся тканей. Лечение гиперплазии эндометрия без выскабливания возможно при легких формах заболевания и включает абляцию (удаление) эндометрия путем диатермокоагуляции или лазерного воздействия.
В тяжелых случаях, не поддающихся медикаментозному лечению, при постоянных кровотечениях, рецидивирующей гиперплазии или при комплексной атипичной форме патологии может быть рекомендовано хирургическое лечение гиперплазии эндометрия – удаление матки.
Удаление полиповидных образований производится с помощью гистероскопии.
Профилактика гиперплазии эндометрия
Для снижения риска этой патологии необходимо:
- в перименопаузальном периоде назначать женщинам эстрогены только в комбинации с гестагенными препаратами;
- при нерегулярных менструациях по назначению врача использовать оральные контрацептивы, нормализующие цикл;
- поддерживать нормальный вес.
Лечение в клинике на Барклая
Терапия гиперплазии эндометрия довольно сложна и зависит от возраста пациентки, тяжести заболевания, выраженности его признаков, возможности принимать препараты, их переносимости и многих других факторов. Такая женщина нуждается в регулярном наблюдении и лечении у гинеколога.
Клиника на Барклая предлагает:
- консультации и лечение у квалифицированных врачей;
- тщательное диагностическое обследование;
- динамическое наблюдение и оценку эффективности лечения;
- подбор наиболее современного и эффективного гормонального препарата;
- психологический комфорт для пациенток, внимательное отношение всего персонала;
- доступные цены на услуги.

Запишитесь на прием к гинекологу по телефону клиники. Помните, что при правильном лечении все пациентки с гиперплазией эндометрия избегают злокачественной трансформации этого заболевания.
Аденомиоз | Симптомы, осложнения, диагностика и лечение
Аденомиоз возникает, когда ткань эндометрия, которая обычно вытягивает матку, врастает в мышечную стенку матки. Вытесненная ткань эндометрия продолжает действовать, как обычно, вызывая утолщение, разрушение и кровотечение во время каждого менструального цикла. Результатом может стать увеличенная матка и болезненные, тяжелые периоды.
Причина аденомиоза остается неизвестной, но болезнь обычно исчезает после менопаузы. Для женщин, которые испытывают серьезный дискомфорт от аденомиоза, некоторые методы лечения могут помочь, но единственным наиболее надежным и эффективным лекарством на сегодняшний день является гистерэктомия.
Симптомы
Иногда аденомиоз происходит спокойно, не вызывая никаких признаков или симптомов, или только легкие неудобства. В других случаях аденомиоз может вызывать:
- Тяжелое или длительное менструальное кровотечение
- Тяжелые судороги или острые, ножевидные боли в области таза во время менструации (дисменорея)
- Менструальные судороги, которые сохраняются в течение всего вашего периода и ухудшаются по мере взросления
- Боль во время полового акта
- Сгустки крови, которые проходят в течение вашего периода
Ваша матка может стать больше. Хотя вы, возможно, не знаете, увеличена ли ваша матка, вы можете заметить, что нижняя часть вашего живота кажется большой или слишком чувствительна.
Причина аденомиоза неизвестна. Экспертные теории о возможной причине включают:
- Инвазивный рост ткани. Некоторые эксперты считают, что аденомиоз является результатом прямого вторжения клеток эндометрия из подкладки матки в мышцу, которая образует стенки матки.
 Разрезы матки, сделанные во время операции, такие как кесарево сечение (С-разрез), могут способствовать прямому вторжению клеток эндометрия в стенку матки.
Разрезы матки, сделанные во время операции, такие как кесарево сечение (С-разрез), могут способствовать прямому вторжению клеток эндометрия в стенку матки. - Происхождение развития. Другие эксперты полагают, что аденомиоз возникает внутри мышцы матки из ткани эндометрия, осажденной там, когда матка сначала образуется у плода.
- Воспаление матки связано с родами. Другая теория предполагает связь между аденомиозом и родами. Воспаление слизистой оболочки матки в послеродовом периоде может привести к нарушению нормальной границы клеток, которые выстилают матку. Хирургические процедуры на матке могут иметь аналогичный эффект.
- Происхождение стволовых клеток. Недавняя теория предполагает, что стволовые клетки костного мозга могут вторгаться в мышцу матки, вызывая аденомиоз.
Независимо от того, как развивается аденомиоз, его рост зависит от циркулирующего эстрогена в организме женщины. Когда производство эстрогенов уменьшается при менопаузе, аденомиоз в конечном итоге уходит.
Факторы риска аденомиоза включают:
- Перед маточной операцией, такой как удаление С-секции или удаление фибромы
- Роды
- Переходный возраст
Большинство случаев аденомиоза, которые зависят от эстрогена, встречаются у женщин в возрасте от 40 до 50 лет. Аденомиоз у женщин среднего возраста может относиться к более длительному воздействию эстрогена по сравнению с более молодыми женщинами. До недавнего времени аденомиоз чаще всего диагностировался только тогда, когда у женщины была гистерэктомия. Современные исследования показывают, что это состояние может быть общим, но часто необнаруженным, у молодых женщин.
Осложнения
Если у вас часто бывает продолжительное, сильное кровотечение во время менструального цикла, может произойти хроническая анемия. Анемия вызывает усталость и другие проблемы со здоровьем. Если вы подозреваете, что у вас может быть анемия, обратитесь к врачу.
Если вы подозреваете, что у вас может быть анемия, обратитесь к врачу.
Хотя подобное состояние и не является вредным, боль и чрезмерное кровотечение, связанное с аденомиозом, могут нарушить ваш образ жизни. Возможно, вы избегаете действий, которые вам нравились в прошлом, потому что не знаете, когда и где можете начаться кровотечение.
Болезненные менструальные циклы могут заставить вас пропустить работу или школу и могут создать конфликт в отношениях. Периодическая боль может привести к депрессии, раздражительности, беспокойству, гневу и чувству беспомощности. Вот почему важно обратиться к врачу, если вы подозреваете, что у вас может быть аденомиоз.
Диагностика
Врач может подозревать аденомиоз на основе:
- Признаки и симптомы
- Тазовый осмотр, который показывает увеличенную чувствительную матку
- Ультразвуковая визуализация матки
- Магнитно-резонансная томография (МРТ) матки
В некоторых случаях врач может взять образец ткани матки для тестирования (биопсия эндометрия), чтобы убедиться, что аномальное маточное кровотечение не связано с каким-либо другим серьезным заболеванием. Но биопсия эндометрия не поможет врачу подтвердить диагноз аденомиоза. Единственный способ быть уверенным в аденомиозе — это осмотреть матку после операции, чтобы удалить ее (гистерэктомия).
Другие заболевания матки могут вызывать признаки и симптомы, сходные с аденомиозом, что затрудняет диагностику аденомиоза. Такие состояния включают в себя фиброзные опухоли (лейомиомы), маточные клетки, растущие за пределами матки (эндометриоз), и рост в маточной оболочке (полипы эндометрия). Ваш врач может заключить, что у вас есть аденомиоз только после определения нет ли других возможных причин для ваших признаков и симптомов.
Лечение
Аденомиоз обычно уходит после менопаузы, поэтому лечение может зависеть от того, насколько вы близки к этому этапу жизни.
Варианты лечения аденомиоза включают:
- Противовоспалительные препараты. Если вы приближаетесь к менопаузе, врач может выписать противовоспалительные препараты, такие как ибупрофен (Advil, Motrin IB, другие), чтобы контролировать боль. Начав прием противовоспалительное лекарства за два-три дня до начала вашего цикла и продолжая принимать его во время цикла, вы можете уменьшить менструальный кровоток и помочь облегчить боль.
- Гормональные препараты. Комбинированные противозачаточные таблетки для эстроген-прогестина или вагинальные кольца могут уменьшить сильное кровотечение и боль, связанные с аденомиозом.
- Гистерэктомии. Если боль тяжелая, а до менопаузы ещедовольно далеко, врач может предложить операцию по удалению матки (гистерэктомия). Удаление яичников не требуется для контроля аденомиоза.
Гиперплазия эндометрия | Цены на операцию в клинике «Здоровая Женщина»
Операционное лечение гиперплазии эндометрия в Москве
При разрастании слизистой оболочки матки происходит нарушение работы всей репродуктивной системы. Такое заболевание может иметь различные причины, формы и требует срочного лечения. В клинике «Здоровая Женщина» вам проведут операцию при гиперплазии эндометрия по доступной цене с применением самых современных методик. Наш медицинский центр включает штат высококвалифицированных врачей, обладает современным диагностическим и операционным оборудованием, применяет лазерные технологии. Мы поможем вам справиться с любой проблемой и позаботиться о женском здоровье.
Классификация
Сколько стоит операция при гиперплазии эндометрия, зависит от формы и степени заболевания. Выделяют два основных вида:
- Типичный (доброкачественный). В этом случае разрастание маточных желез происходит в результате гормонального дисбаланса.
- Атипичный. При этой форме происходит мутация клеток эпителия.
 Заболевание в такой форме не связано с гормональным фоном и нередко является предраковым состоянием, влекущим за собой образование злокачественной опухоли.
Заболевание в такой форме не связано с гормональным фоном и нередко является предраковым состоянием, влекущим за собой образование злокачественной опухоли.
В любом случае заболевание требует срочного лечения. В нашей клинике вам проведут диагностику на высоком уровне и точно определят форму и степень заболевания.
Причины и симптомы
У возникновения гиперплазии эндометрия могут быть различные причины, чаще всего связанные с гормональными сбоями. Наиболее частыми факторами являются:
- хирургические аборты и выскабливание матки;
- бесконтрольный прием оральных контрацептивов;
- сбои в работе иммунной системы;
- длительная гормонотерапия;
- поликистоз, опухоли и другие заболевания яичников;
- хроническая артериальная гипертензия;
- ожирение и сбои в работе других систем организма.
Наиболее часто пациентки клиники при гиперплазии эндометрия жалуются на:
- маточное кровотечение;
- длительные задержки менструации;
- мажущие выделения из влагалища бурого цвета;
- повышение болезненности менструаций, увеличение объема кровянистых выделений.
Развитие гиперплазии эндометрия угрожает возникновению осложнений, имеющих серьезные последствия:
- бесплодие;
- невынашивание беременности;
- хронические воспалительные процессы;
- мастоплазия и миоматоз;
- рак эндометриоидной ткани.
Поэтому очень важно своевременно обратиться к врачу и пройти курс лечения. Наша клиника в Москве проводит операции при гиперплазии эндометрия по доступным ценам.
Способы лечения
В зависимости от формы и стадии болезни применяются различные виды операций. Наша клиника предлагает современные методики, позволяющие эффективно и минимально травматично решить проблемы с женским здоровьем.
- Выскабливание (кюретаж). С помощью специальных инструментов врач выскабливает верхний слой эпителия. Процедура проводится с применением гистероскопии, позволяющей контролировать процесс.
 Назначается при железисто-кистовой гиперплазии эндометрия, а также при его толщине не более 16 мм.
Назначается при железисто-кистовой гиперплазии эндометрия, а также при его толщине не более 16 мм. - Криодеструкция. Этот способ основан на воздействии жидким азотом на места развития патологии. Это одна из эффективных методик, позволяющая не травмировать здоровые ткани. Назначается при противопоказаниях к предыдущему методу, а также при атипичной форме заболевания.
- Лазерная абаляция. При регулярных рецидивах болезни назначается удаление патологически разрастающихся участков эпителия с помощью лазерного оборудования. Процедура практически не доставляет дискомфорта, не затрагивает здоровые ткани, позволяет снизить риск осложнений.
- Удаление матки. Когда гиперплазия эндометрия достигает значительных размеров и аденоматоз находится на последних стадия, щадящие методики могут оказаться неэффективными. В этом случае необходимо удаление матки. Это особенно важно при атипичной форме, поскольку такое заболевание может перерасти в онкологию.
Обращаясь к нам, вы можете рассчитывать на квалифицированный и внимательный персонал. Команда опытных врачей найдет оптимальный способ решения вашей проблемы, а современное оборудование, применяемое в нашей клинике, позволит сократить период реабилитации и сделать операцию безболезненной. Записаться на прием к специалисту в медицинский центр «Здоровая Женщина», чтобы проконсультироваться по вопросу гиперплазии эндометрия, вы можете по телефону, указанному на сайте.
Гиперплазия эндометрия матки: лечение и диагностика в Одессе
Под гиперплазией матки принято понимать чрезмерное разрастание ее слизистой оболочки. Сбой в этой части организма обусловлен гормональными нарушениями. Слизистая оболочка теряет способность к уменьшению после окончания цикла и приобретает гипертрофированный вид. Симптомы заболевания — нарушения менструального цикла, мажущие выделения и обильные месячные.
Однако часто болезнь протекает без ярко выраженных симптомов. Проблема разрастания эндометрия матки актуальна для 50% женщин от 30 до 39 лет.
«Тихое», но опасное заболевание требует высокого профессионализма доктора и передовых методов диагностики. Все это вы найдете в медицинском доме Odrex, где вам предложат:
- Высокоточную диагностику с применением гистероскопа Karl Storz без наркоза и боли;
- Оперативное составление плана индивидуального лечения;
- Работающие методы лечения.
Диагностика гиперплазии эндометрия в Odrex
Первый и обязательный шаг в диагностике гиперплазии – осмотр женщины врачом-гинекологом. В ходе осмотра врач назначит нужные лабораторные и инструментальные исследования.
Сегодня во врачебной практике применяются высокоэффективные и щадящие методы диагностики:
- УЗИ органов малого таза – распространенный метод. Современные аппараты помогают увидеть и измерить толщину слоя слизистой оболочки с точностью до десятых миллиметра. При этом сама по себе, не подтвержденная другими исследованиями, картина УЗИ – это не диагноз. Делать УЗИ нужно или в середине цикла или сразу по окончании месячных.
- МРТ органов малого таза обеспечивает наглядную визуализацию, благодаря четкому контрасту мягких тканей. Незаменимый инструмент для выявления опухолевых заболеваний. Магнитный резонанс точно диагностирует спаечный процессв малом тазу, что невозможно сделать только с помощью ультразвукового исследования.
- Гистероскопия – наиболее информативный метод, обеспечивающий точные и достоверные результаты. На вооружении нашей клиники немецкая оптическая система Karl Storz, которая выполнит прицельную биопсию в том месте, где расположен очаг разрастания клеток. При необходимости производится срезание патологической ткани. Занимает процедура менее часа и требует госпитализации на полдня. Срок гистологического исследования – от 2 до 14 дней.
- Лабораторные анализы на определение уровня гормонов в крови, надпочечниках и щитовидной железе.

Подозрение на гиперплазию появляется, когда толщина эндометрия больше 15-16 мм (по данным УЗИ или МРТ органов малого таза).
Как лечить гиперпластический процесс?
На лечение гиперплазии эндометрия влияет много факторов. Среди них решающее значение имеет вид гиперплазии эндометрия:
- Простая железистая гиперплазия характеризуется избыточным разрастанием ткани эндометрия.
- Аденоматозная или комплексная гиперплазия, при которой внутри эндометрия образуются не характерные для него структуры. Встречается примерно у трех из ста женщин.
- Железисто кистозная гиперплазия эндометрия. Сопровождается образованиями кистозного характера и провоцирует увеличение объема матки.
- Очаговая гиперплазия (полипы эндометрия). Патологические образования, состоящие из тела и ножки.
- ААтипическая гиперплазия эндометрия — самая опасная разновидность, которая часто приводит к злокачественным образованиям. Принято выделять очаговую и диффузную разновидности. Иногда к этой форме приводит неправильно подобранная терапия железистой гиперплазии.
Главный принцип лечения основан на удалении участка патологической слизистой. С этой целью в медицине были разработаны следующие методы:
- Гистероскопическая резекция (срезание) эндометрия и удаление полипов — обязательный первый этап лечения. К достоинствам такого лечения относится малая травматичность, экономичность (благодаря сокращению времени нахождения в клинике), сохранение репродуктивной функции и уменьшение длительности вмешательства.
- Гормональная терапия, которая заключается в приеме препаратов, нормализующих выработку эстрогена и прогестерона. Существуют препараты общего и местного воздействия (внутриматочные). Разработано множество схем приема подобных лекарственных препаратов, и задача врача – выбрать оптимальный вариант.
- Хирургическое вмешательство кюретаж, или в просторечии – выскабливание. Сегодня считается устаревшим методом. Смысл процедуры понятен из названия.
 Такой операции присущи многочисленные недостатки: сильные болевые ощущения, необходимость большого расширения шейки матки. риск возникновения спаечного процесса в малом тазу. Проводится под общим наркозом. Необходимость в госпитализации зависит от физического состояния пациента и способности переносить наркоз. Возможен местный наркоз обезболивающими препаратами.
Такой операции присущи многочисленные недостатки: сильные болевые ощущения, необходимость большого расширения шейки матки. риск возникновения спаечного процесса в малом тазу. Проводится под общим наркозом. Необходимость в госпитализации зависит от физического состояния пациента и способности переносить наркоз. Возможен местный наркоз обезболивающими препаратами. - Удаление матки или гистерэктомия — радикальный способ, который применяется исключительно при атипической гиперплазии. когда велик риск перерождения доброкачественных образований в злокачественные, или при рецидивирующей форме заболевания, не нуждающейся в терапии.
Помните, что лечение этой болезни носит индивидуальный характер. Нет единой панацеи, которая бы работала со стопроцентной гарантией во всех случаях без исключения. И только опытный гинеколог-эндокринолог определит ту схему, дозу и продолжительность лечения, которые «сработают» в каждом конкретном случае. Однако преимущественно назначается комбинированное лечение, которое подразумевает и хирургическое вмешательство, и гормональную терапию.
Вопрос — ответ
Работают ли народные средства лечения гиперплазии?
Сегодня на просторах интернета встречается масса рекомендаций, как вылечить гиперплазию пиявками, чистотелом, лопухом или крапивой. Однако эффективность этих способов в отношении этого заболевания в официальной медицине не подтверждена. Поэтому не стоит рисковать здоровьем из-за сомнительных рецептов.
Возможны ли рецидивы болезни?
Риск повторного возникновения этого заболевания велик и возникает в 30 % процентов случаев. При этом прогнозировать возникновения рецидива невозможно: он не зависит ни от течения заболевания, ни от выбранной схемы лечения. Поэтому проведение биопсии эндометрия спустя 3-6 месяцев после окончания лечения — обязательная процедура.
Можно ли забеременеть при ГПЭ?
При болезни может отсутствовать овуляция, и сама слизистая оболочка иногда в не состоянии принять эмбрион. При этом после удачно проведенного лечения забеременеть естественным образом возможно. Детородная функция восстанавливается практически всегда. Поэтому если в планах женщины родить здорового и крепкого малыша, вылечить гиперплазию следует обязательно.
При этом после удачно проведенного лечения забеременеть естественным образом возможно. Детородная функция восстанавливается практически всегда. Поэтому если в планах женщины родить здорового и крепкого малыша, вылечить гиперплазию следует обязательно.
Как предупредить возникновение гиперплазии эндометрия?
Профилактические рекомендации в этом случае носят общий характер без специфических моментов. Это и регулярные визиты к гинекологу, и лечение воспалительных половых заболеваний, и занятия спортом.
Может ли гиперплазия «пройти сама»?
Помните, что гиперплазия эндометрия — потенциальный рак. Это доказано авторитетными зарубежными и отечественными исследователями. Не стоит надеяться, что разросшаяся слизистая «рассосется» сама собой. Без врачебной помощи это заболевание пройти не может.
Современные аспекты профилактики и лечения гиперпластических процессов эндометрия в перименопаузе
Современные аспекты профилактики и лечения гиперпластических процессов эндометрия в перименопаузе
Профессор, д.м.н. И.Б. Манухин, профессор, д.м.н. А.Л. Тихомиров,
С.М. Шаркова, А.А. Кочарян
Гиперпластические процессы эндометрия являются распространённой гинекологической патологией, частота которой существенно увеличивается к периоду возрастных гормональных перестроек в перименопаузальном возрасте. Имея неодинаковую степень развития, гиперпластические процессы нередко становятся благоприятным фоном для возникновения предрака, а затем и рака эндометрия, что в течении многих десятилетий представляет важную медико — социальную проблему.
В настоящее время всё более актуальной становится проблема сохранения здоровья женщины перименопаузального возраста, что связано с увеличением средней продолжительности жизни, возрастающей доли женщин старшей возрастной группы среди населения.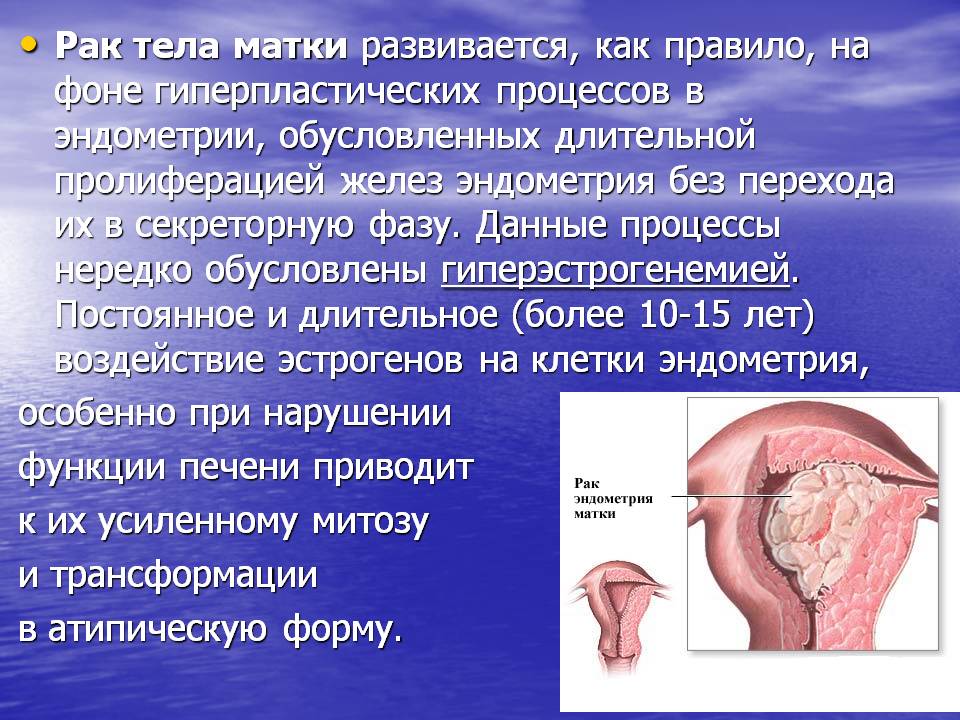
Ещё 50 — 60 лет назад только 28% женщин доживали до возраста менопаузы и лишь 5% из них достигали возраста 75 лет. В настоящее время 95% женщин достигает периода перименопаузы, а 55% из них достигает 75 летнего возраста [3 7 12].
Современная демографическая ситуация в стране и мире такова, что 90% женщин проводят в постменопаузальном периоде треть своей жизни. К 2007 году 12% населения мира составляют лица старше 65 лет [3 7 12].
Термин перименопауза — означает период жизни женщины от первого нарушения регулярности менструального цикла до наступления аменореи.
Этот период характеризуется появлением биологических, клинических и эндокринных признаков прекращения менструаций. Паталогические маточные кровотечения среди женщин перименопаузального возраста составляют от 2 до 5% от всех гинекологических больных и являются достаточно распространенным симптомом, который наблюдается при различных патологических процессах эндометрия:
— гиперпластические процессы эндометрия,
— миома матки, аденомиоз,
— гормонально-активные опухоли яичников и их различное сочетание [4 9,10,].
У большинства женщин период перименопаузы (климактерический период) приходится на возраст 45 -50 лет. Кровотечения в этом возрасте именуются климактерическими, что подчеркивает их связь с возрастными изменениями в репродуктивной системе.
Особая роль в гормональной перестройке отведена гипоталямусу, с началом перименопаузы появляется лабильность менструального цикла, нарушение фазности менструаций, что обусловливает нарушение длинной обратной связи как на уровне гипофиза, так и гипоталямуса. Наиболее стабильная корреляция между ФСГ и ЛГ установленная в репродуктивном периоде, в перименопаузе отсутствует.
Со стороны функции яичников в период перименопаузы происходит снижение эстрогенов и прогестерона [4 .9, 10, 11, 13, 14].
Ряд авторов сообщает об отсутствии достоверных статистических различий содержания в крови пролактина, тестостерона и эстрадиола у здоровых женщин, как в репродуктивном периоде, так и в период перименопаузы [7 . 12].
12].
Продукция половых стероидных гормонов у женщин тесно связана с ростом фолликулов и гаметогенезом.
Гонадотропная функция гипофиза при физиологическом течении периода перименопаузы является разнонаправленной: уровень ФСГ и ЛГ повышается, а уровень пролактина снижается, что можно рассматривать как универсальную реакцию на резкое снижение функции яичников. При сравнении уровня содержания в крови гормонов: на 7 — 9 день цикла у женщин в перименопаузе ЛГ в три раза, а ФСГ в девять раз выше уровня содержания в крови здоровых женщин репродуктивного возраста, в соответствующие дни менструального цикла [13,14, 15].
Эстрадиол, обнаруживаемый в крови у женщин в перименопаузе, является в основном продуктом экстрагландулярного превращения андрогенов в эстрогены, что имеет важное значение для поддержания нормального гомеостаза.
Ароматизирующие фементные системы, способные превращать андростендион и тестостерон в эстрадиол, обнаруживаются главным образом в жировой ткани.
Ароматизация андростендиона происходит в стромальных и сосудистых клетках жировой клетчатки, а сами жировые клетки (адипоциты) активно захватывают его из плазмы и являются депо половых гормонов [4. 9,10].
Гиперпластические процессы, развивающиеся у женщин в период перименопаузы, имеют неодинаковую степень развития, иногда приобретают характер предракового заболевания.
Согласно классификации ВОЗ (Женева 1984 г .), выделяют три основных вида гиперпластических процессов в эндометрии:
— эндометриальные полипы;
— эндометриальная гиперплазия;
— атиптческая гиперплазия эндометрия.
В отечественных материалах обычно используется морфологическая классификация Б.И.Железнова ( 1973 г .), которая выделяет:
— железистую гиперплазию эндометрия;
— железисто — кистозную гиперплазию эндометрия;
— атиптческую гиперплазию эндометрия (диффузные аденоматозные изменения, очаговый аденоматоз и аденоматозные полипы).
Каждое из этих заболеваний может стать причиной кровянистых выделений у женщин в период перименопаузы.
Частота озлокачествления гиперпластических процессов эндометрия колеблется в достаточно широких пределах (0,25 — 50%) и определяется морфологическими особенностями заболевания, длительностью его рецидивирования, а также возрастом пациентки [1. 4,8].
В литературе данная проблема широко обсуждалась, детально освещены вопросы этиологии и патогенеза, диагностики и лечения гиперпластических процессов Несмотря на появление новых направлений в ведении больных с гиперпластическими процессами эндометрия в различных современных периодах , вопросы лечения данной патологии остаются одними из наиболее актуальных вопросов гинекологии, и ещё далеки от окончательного решения. Это обусловлено прежде всего сложным и неоднородным пато- и морфогенезом заболевания и индивидуальной чувствительностью организма к различным лечебным воздействиям [1. 4,].
Остается недостаточно изученной зависимость различных морфологических форм гиперпластических процессов эндометрия от нейро — эндокринных нарушений организма, таких, как позднее наступление менопаузы, клинический и субклинический сахарный диабет, ожирение, бесплодие, гипертоническая болезнь [8].
Разработка морфологических критериев индивидуальной чувствительности доброкачественных гиперпластических процессов и предрака эндометрия имеет важное практическое значение для оптимизации способа лечения, определения показаний к гормонотерапии, а следовательно и повышения эффективности профилактики развития и лечения предрака, рака эндометрия [1. 4,].
Практически все авторы едины в мнении, что изменение гормональных взаимоотношений играет роль в развитии пролиферативных процессов в эндометрии. Эндометрий, как «ткань мишень», испытывающий на себе влияние половых гормонов, чрезвычайно чувствителен к действию эстрогенов, оказывающих эффект на его структуру и функцию.
Эстрогены — основной фактор, вызывающий пролиферацию эндометрия, которая при отсутствии достаточного влияния прогестерона, прогрессирует в железистую и атиптческую гиперплазию.
К нарушению взаимоотношений между прогестероном и эстрогенами и к возникновению относительной гиперэстрогенемии приводит – ановуляция.
В перименопаузе в крови повышается уровень ФСГ и ЛГ, что оказывает стимулирующее действие на функцию яичников, которые отвечают повышенной продукцией эстрогенов, не компенсированных действием прогестерона. Следствием этого является нередкое сочетание гиперпластических процессов эндометрия с миомой матки и эндометриозом у женщин указанной возрастной группы [4. 7. 8. 13].
Доказано, что характер пролиферации эндометрия, обусловлен не только уровнем содержания в крови и соотношением гормонов, но и способностью эндометрия к их связыванию, — то есть количеством и качеством специфических рецепторов.
Можно полагать, что генетически обусловленный дефицит рецепторов прогестерона и рецепторов эстрадиола, либо нарушение этой рецепторной системы под влиянием различных патогенетических факторов являются одной из причин неэффективности гормонального лечения.
Между тем, в настоящее время не существует методик, позволяющих в клинических условиях осуществлять полноценную коррекцию нарушений рецепторного аппарата эндометрия. В клинической практике широко исследуется изучение фоновых и предраковых состояний эндометрия [3.7.12.].
Известно, что длительная пролиферация клеток эндометрия независимо от причины вызвавшую пролиферацию, облегчает реализацию онкогенного фактора [1.].
За последние 20 лет в России заболеваемость раком эндометрия (тела матки) выросла в два раза [7].
Это связано не только с увеличением средней продолжительности жизни, но и с нарастанием в популяции обменно — эндокринных заболеваний, таких как ановуляция, бесплодие, ожирение, гипертоническая болезнь, сахарный диабет [4].
Рост заболеваний раком тела матки требует не только усовершенствования методов лечения больных, но и в первую очередь усовершенствование возможной профилактики и лечения патологических заболеваний эндометрия на этапе его доброкачественных изменений.
Риск малигнизации в случае железисто — кистозной гиперплазии эндометрия (ЖГЭ) и полипов эндометрия составляет 1 — 2%, что позволяет отнести их скорее к фоновым заболеваниям нежеле к предраковым. В то же время у 55,9% больных раком эндометрия в перименопаузе обнаруживались полипы и железистая гиперплазия эндометрия [1.].
На основании только морфологических исследований невозможно составить прогноз риска развития ракового процесса, должен быть оценен фон, на котором возник пролиферативный процесс в эндометрии, то есть нейро — эндокринно — обменные нарушения в организме женщин, их возраст, гинекологический анамнез, клиническое течение, рецидивирование гиперплазии [1.].
Рецидивирующая гиперплазия эндометрия у женщин перименопаузального возраста, развивающаяся часто на фоне ожирения и гипертонической болезни, может быть отнесена к предраку.
В связи с известной зависимостью физиологической трансформации эндометрия от состояния гормональной регуляции, назначение гормональных препаратов для профилактики и лечения гиперпластических процессов эндометрия (ГПЭ) в перименопаузальном периоде считается патогенетически обоснованным.
В настоящее время здоровье, качество жизни и общий жизненный прогноз у женщин в период климактерия определяется прежде всего адекватностью и современностью лечебно — профилактических мероприятий, среди которых гормональная терапия играет большую роль [7].
Однако при отрицательном отношении пациенток к приёму гормональных препаратов в период климактерия, не стоит забывать и о возможности применении препаратов содержащих в своем составе фитогормоны и фитоэстрогены с целью возможной профилактики развития многих заболеваний развивающихся в этом возрастном периоде. «Данные препараты устраняют также раннюю вазомоторную и психоэмоциональную симптоматику, метаболические нарушения, явления остеопороза, сердечно — сосудистых заболеваний и других заболеваний, развивающихся в климактерии.» [7]
Лечебная тактика при гиперпластических процессах зависит от патоморфологической характеристики эндометрия, возраста, этиологии и патогенеза заболевания, сопутствующей генитальной и экстрагенитальной патологии.
Основным методом лечения гиперпластических процессов эндометрия в период перименопаузы, после оценки патоморфологического исследования, сопутствующей гинекологической и соматической патологии, является гормонотерапия с оказанием антиэстрогенного влияния на слизистую оболочку полости матки, с использованием препаратов, обладающих прогестероновой активностью — синтетические прогестины, «чистые» гестагены. Применяют их укороченными курсами, общей продолжительностью лечения 6 месяцев .
Назначению гормональных препаратов предшествует гистологическое исследование эндометрия, полученного в результате РДВ.
Использование в терапии препаратов прогестероноподобного действия (дюфастон, ЛРС «Мирена», норколут, прогестерон 1% и др.) обосновывается биологическими эффектами прогестерона.
Прогестерон предотвращает эстрогениндуцированное клеточное деление, и тем самым создает условия, при которых пролифирирующий эндометрий превращается в секреторный. Сущность биологического действия прогестерона проявляется в антиэстрогенном эффекте, который осуществляется двумя механизмами:
1 — уменьшение количества цитозольных рецепторов эстрадиола путем ингибирования их синтеза;
2 — прогестерон индуцирует 17в — гидроксистероиддегидрогеназу, которая превращает эстрадиол в менее активный эстрон.
Следует заметить, что реализация действия прогестерона и прогестероноподобных веществ на местном уровне возможна лишь при наличии достаточного количества рецепторов прогестерона. Гормональное лечение гиперпластических процессов эндометрия, проявляющихся маточными кровотечениями, проводится с целью достижения нескольких эффектов, которые связаны между собой:
1) остановка кровотечения;
2) прекращение патологической пролиферации эндометрия;
3) нормализация взаимоотношений в гипоталямо — гипофизарно — яичниковой системе.
Для достижения стойкого клинического эффекта лечение синтетическими прогестинами рекомендуется продолжать 6 — 12 месяцев [11. 12].
12].
Влияние гормонов на клетки реализуется посредством взаимодействия со специфическими рецепторами. Количество рецепторов зависит от концентрации соответствующего гормона и от количества стероидов других классов [9.10.].
Эстрогены стимулируют пролиферацию клеток эндометрия, развитие секреторного аппарата клеток и синтез рецепторов к эстрогенам и прогестерону [15].
В тканях мишенях эстрогены увеличивают концентрацию собственных рецепторов и цитоплазматических рецепторов к прогестерону и андрогенам. Прогестерон блокирует этот механизм, снижая, таким образом, количество рецепторов к эстрогенам.
Кроме этого, прогестерон ускоряет оборот ранее синтезированных рецепторов.
Рецептор прогестерона состоит из А и В субъединиц, в соотношении 1:1. Прогестерон обладает высоким сродством к своему рецептору. Эстрадиол, кортизол и тестостерон имеют незначительное сродство к прогестероновым рецепторам. Прогестерон не имеет сродства к рецепторам эстрогенов, но некоторые прогестины и их метаболиты взаимодействуют с эстрагеновыми рецепторами [15].
Эдометрий способен к стероидогенезу, вырабатывая на местном уровне эстрадиол и сульфат эстрона, пролактин, простагландины, андрогены, маркерные протеины. Кроме того он вырабатывает факторы роста — эпидермальный фактор роста, инсулиноподобный фактор роста (ИПФР) — 1 и 2, трансформирующие факторы роста 1-а и 1-в и их рецепторы [13, 16].
ИПФР — 1 и ИПФР — 2 структурно относятся к инсулину. Считается, что ИПФР, действуя через аутокринные и паракринные механизмы вызывает пролиферацию и дифференцировку клеток. В крови ИПФР находится в связи с белком — переносчиком, известно 6 белковых переносчиков (ИПФРСП). Наибольший интерес представляет ИПФРСП — 1, который синтезируется и секретируется в эндометрии во вторую фазу менструального цикла и прогестерон индуцирует его синтез.
Морфологические изменения эндометрия в секреторной фазе характеризуются отёком стромы, атрофией желез, децидуализацией стромы вплоть до полной атрофии функционального слоя и отсутствие митозов [16]. Наблюдается инфильтрация тканей лимфоцитами, плазматическими клетками и макрофагами, иногда возникает некроз стромы. Выявлены выраженные изменения со стороны сосудов эндометрия, заключающиеся в утолщении стенок артериол, тромбозе капилляров и уменьшении количества спиралевидных артерий.
Наблюдается инфильтрация тканей лимфоцитами, плазматическими клетками и макрофагами, иногда возникает некроз стромы. Выявлены выраженные изменения со стороны сосудов эндометрия, заключающиеся в утолщении стенок артериол, тромбозе капилляров и уменьшении количества спиралевидных артерий.
Так, например, в результате проведенных исследований, посвященных влиянию левоноргестрела (производного 19 — нортестостерона), входящего в ЛРС, было выявлено значительное снижение эстрогеновых и прогестероновых рецепторов эндометрия [13, 14, 15].
Кроме того, в 1998г. Н.О.С ritchley и соавт. опубликовали исследования по изучению содержания прогестероновых и эстрогеновых рецепторов, А и В субъединиц и простагландин — дегидрогеназы в эндометрии на фоне применения ЛРС.
Полученные данные свидетельствуют о значительном снижении количества эстрогеновых, а также А и В субъединиц прогестероновых рецепторов.
При этом наблюдается более выраженная супрессия В субъединицы рецепторов к прогестерону. Кроме того, совместно с ингибированием прогестероновых рецепторов было выявлено значительное снижение уровня простагландин — дегидрогеназы. А также выявлено подавление синтеза, индуцированных эстрогенами и прогестероном ростовых факторов [15].
В противоположность этому зарегистрировано стимулирующее действие левоноргестрела, входящего в ЛРС на образование циклооксигеназы — 2, рецепторов к пролактину и белка, связывающего ИПФР — 1 и ИПФРСП – 1 [15].
Гестагеновому влиянию на ИПФР(1,2) и ИПФРСП — 1 посвящены многочислен-ные исследования, наибольший интерес из которых представляет работа Rutanen .
В ряде исследований были получены результаты, свидетельствующие о супресорном действии левоноргестрела на ИПФР- 1, одновременно с ингибирующим действием на ИПФРСП — 1 и ИПФР — 2.
Значимость данных исследований была обусловлена определяющей ролью ИПФР — как медиатора эстрогенового влияния на эндометрий. Кроме того, ИПФРСП — 1 является маркером прогестинового влияния на эндометрий, которое выражается в дециадулизации стромы и подавлении роста эндометрия.
Таким образом, ингибирование ИПФР — 1, по всей вероятности является одним из возможных молекулярных механизмов антипролиферативного действия левоноргестрела, входящего в состав ЛРС, на гиперплазированный эндометрий у женщин в период перименопаузы [14, 15].
Для оказания антиэстрогенного влияния на эндометрий, применяют также эстроген-гестагенные препараты (нон-овлон, ановлар и др.). К их применению существуют относительные противопоказания: хронический холецистит или панкреатит, тромбофлебиты, варикозное расширение вен и др. [4., 13].
Помимо гестагенов, эстраген-гестагенных препаратов, в настоящее время, для лечения гиперпластических процессов эндометрия у больных в период климактерия применяют антигонадотропины — даназол — производные 17а — этилтестостерона по 400-600 мг. ежедневно, гестринон или неместран — производные 19 — норстероидов по 2,5мг. 2 раза в неделю в непрерывном режиме в течении 6 месяцев. Эти препараты обладают выраженным антигонадотропным эффектом, способствуют подавлению функции яичников и, как следствие, вызывают гипоплазию и атрофию эндометрия, что наиболее актуально в позднем периоде климактерия [10.].
Сохраняется значимость включения гестагенов, норстероидов для лечения гиперпластических процессов в перименопаузальном возрасте, вследствие их эффективности и безопасности при кратковременных курсах лечения. При этом в каждом конкретном случае только врач, ориентируясь на индивидуальный статус пациентки, обязан четко определить целевые указания, которые должны быть решены при назначении конкретных гормональных препаратов, динамично отслеживая эффективность и безопасность гормонотерапии, в том числе гибко корректируя возникающие проблемы. (А.Н.Караченцев, Г.А.Мельниченко, 2003г.).
Из вышеизложенного следует, что выбор метода профилактики и лечения патологических процессов эндометрия осуществляется с учетом клинико — анамнестических данных, сопутствующей соматической патологии, наличия противопоказаний для проведения традиционной гормонотерапиии, нередко отрицательное отношение пациенток к приему гормональных препаратов, а также органосохраняющее направление в современной медицине, обусловливает необходимость разработки новых подходов к профилактике развития и лечения гиперпластических процессов эндометрия.
Полипы эндометрия
Полипы эндометрия.
Полипы эндометрия-это заболевание при котором в полости матки происходит патологическое разрастание базального слоя эндометрия.Полипы эндометрия обнаруживаются у 0.5-5 % гинекологических больных в возрасте 35-50 лет.
Полип состоит из клеток эпителия.В его строении различают тело и ножку.Полипы эндометрия классифицируют по формам.В основе классификации лежит структура строения полипа.Основные формы полипов:
Железистые. В состав входит железистый и стромальный компонент, железистый преобладает.Такие полипы распространены у женщин репродуктивного возраста.
Железисто-фиброзные.В строении: небольшое количество желез, соединительная ткань, у основания плотная фиброзная ткань.Могут выявляться у всех возрастных категорий.
Фиброзные.Состоят из соединительной ткани с единичными железами.Чаще диагносцируются у женщин пожилого возраста.
Аденоматозные и полипы с очаговым аденоматозом.Состоят из железистой ткани с пролиферацией эпителия.Такие полипы могут иметь в своей структуре атипичные клетки,поэтому их называют предраковыми полипами. Эти полипы имеют особую опасность для женского здоровья .
Что влияет на возникновение полипов эндометрия?
На гиперпластическое разрастание эндометрия , в результате которого образуются полипы, могут влиять разнообразные факторы.Перечислим основные из них.
1.Оперативные вмешательства на органах малого таза во время которых было выскабливание полости матки с диагностическими и лечебными целями.Сюда можно отнести выкидыши, аборты, роды осложненные неполным отделением плаценты.Причины возникновения полипов после хирургических вмешательств –создаются благоприятные условия для инфицирования эндометрия и возникновения хронического воспалительного процесса в слизистой матки.
2.Снижение общего иммунитета.
3.Гормональный дисбаланс-чрезмерная выработка эстрогена и низкий уровень прогестерона.
4.Хронические инфекции органов малого таза воспалительного характера.
5.Нарушение психоэмоционального статуса ( длительные депрессии,сильные стрессовые ситуации).
6.Длительное ношение внутриматочного контрацептива.
7.Нарушения эндокринного характера (дисфункция щитовидной железы).
8.Ряд эктрагенитальных заболеваний: гипертоническая болезнь. Ожирение, сахарный диабет.
9.Наследственная предрасположенность к опухолевидным образованиям.
По каким симптомам можно определить заболевании?
Многие гинекологи отмечают, что при небольших размерах полипов ( до 1 см.), женщины могут не иметь жалоб.Довольньно часто такие полипы обнаруживаются при проведении УЗИ полости матки.Как правило первые жалобы появляются при увеличении размеров полипа.В репродуктивном возрасте беспокоит нарушение менструального цикла(обильные или продолжительные менструации). В период отсутствия менструаций у женщин могут появляться кровянистые или мажущие выделения из половых путей, которые бывают однократными или повторяющимися. У практически здоровых женщин до 45 лет не наступает беременность.Из половых путей периодически могут появляться выделения белого цвета. После полового акта иногда появляются незначительные кровянистые выделения из влагалища.Данный тип выделений называют контактным.Боли внизу живота могут появляться при некротических изменениях в полипе и при рождении полипа.
Данные симптомы имеют сходство с рядом других гинекологических заболеваний,Поэтому очень важно поставить правильный диагноз для того чтобы подобрать соответствующее лечение. Симптомы полипов эндометрия похожи на симптомы следующих заболеваний-эндометриоз ,миома матки, угроза выкидыша в первом триместре беременности.
Как видите . полипы эндометрия очень важно отличать от других гинекологических заболеваний.Современные методы диагностики дают такую возможность.
УЗИ органов малого таза- при исследовании выявляется расширение полости матки .Полипы видны как образования однородной структуры с четким контуром часто повышенной эхогенности.
Гистероскопия считается наиболее точным и информативным методом .Позволяет оценить форму, размеры,расположение полипа, а также оценить стенки матки, дно и трубные углы.Одновременно с диагностикой можно провести удаление полипа.
Гистологический анализ соскоба эндометрия-подтверждает наличие полипа,его структуру, форму.
Как удаляют полипы.
При гистероскопии специальными инструментами производят удаление полипов в полости матки, затем выполняется выскабливание полости матки и цервикального канала
При гистерорезектоскопии специальной электропетлёй удаляется полип и его ножки .Это необходимо для профилактики рецидивов. Полученный материал из полости матки и цервикального канала отправляется на гистологическое исследование.Выполняется контрольное УЗИ органов малого таза ч\з 3-4 дня после операции.
У большинства пациенток восстановительный период после операции проходит довольно спокойно.В течении 10 дней после выскабливания могут беспокоить кровянистые выделения различной интенсивности, чаще умеренные.Для профилактики воспалительных осложнений назначается антибактериальная терапия . Первые 3 недели после операции рекомендуется избегать половых контактов,физической нагрузки, переохлаждения.
Следующий этап лечения определяется возрастом пациентки, структурой полипа, есть ли у нее нарушение менструального цикла.
Если полип фиброзный и нарушений менструального цикла нет, достаточно гистероскопии , удаление полипа, выскабливание полости матки и цервикального канала.При железистой и железисто-фиброзной форме полипа и с нарушением менструального цикла, пациентке возможно рекомендуют гормональное лечение. При аденоматозных полипах и полипах с очаговым аденоматозом пациенткам после консультации онколога рекомендуется хирургическое лечение.Женщинам от 45 лет-удаление матки. Если у пациенки выявлены обменно-эндокринные нарушения, а также есть факторы риска онкологической настороженности, выполняется удаление матки с придатками.
Прфилактика полипов эндометрия предполагает своевременное лечение гиперплазии эндометрия и ограничение повреждающих локальных воздействий на матку.
Аденомиоз: симптомы, причины и лечение
Аденомиоз — это состояние, при котором внутренняя оболочка матки (эндометрий) прорывается через мышечную стенку матки (миометрий). Аденомиоз может вызывать менструальные спазмы, снижение давления в животе и вздутие живота перед менструацией, а также обильные месячные. Заболевание может располагаться по всей матке или локализоваться в одном месте.
Хотя аденомиоз считается доброкачественным (не опасным для жизни) состоянием, частая боль и сильные кровотечения, связанные с ним, могут отрицательно сказаться на качестве жизни женщины.
Каковы симптомы аденомиоза?
Хотя у некоторых женщин с диагнозом аденомиоз симптомы отсутствуют, болезнь может вызывать:
- Обильные длительные менструальные кровотечения
- Сильные менструальные спазмы
- Абдоминальное давление и вздутие живота
У кого возникает аденомиоз?
Аденомиоз — распространенное заболевание. Чаще всего диагностируется у женщин среднего возраста и женщин, родивших детей. Некоторые исследования также предполагают, что женщины, перенесшие операцию на матке, могут иметь риск аденомиоза.
Хотя причина аденомиоза неизвестна, исследования показали, что различные гормоны, в том числе эстроген, прогестерон, пролактин и фолликулостимулирующий гормон, могут вызывать это состояние.
Диагностика аденомиоза
До недавнего времени единственным окончательным способом диагностики аденомиоза было выполнение гистерэктомии и исследование ткани матки под микроскопом. Однако технология визуализации позволила врачам распознать аденомиоз без хирургического вмешательства.С помощью МРТ или трансвагинального УЗИ врачи могут увидеть особенности заболевания в матке.
Если врач подозревает аденомиоз, первым делом он должен пройти медицинский осмотр. Осмотр органов малого таза может выявить увеличенную и болезненную матку. Ультразвук может позволить врачу увидеть матку, ее слизистую оболочку и мышечную стенку. Хотя УЗИ не может точно диагностировать аденомиоз, оно может помочь исключить другие состояния с аналогичными симптомами.
Другой метод, который иногда используется для оценки симптомов, связанных с аденомиозом, — соногистерография.В соногистерографии физиологический раствор вводится через крошечную трубку в матку во время ультразвукового исследования.
МРТ — магнитно-резонансная томография — может использоваться для подтверждения диагноза аденомиоза у женщин с аномальным маточным кровотечением.
Поскольку симптомы очень похожи, аденомиоз часто ошибочно принимают за миому матки. Однако эти два условия не совпадают. В то время как миома представляет собой доброкачественную опухоль, растущую в стенке матки или на ней, аденомиоз представляет собой меньшую определенную массу клеток в стенке матки.Точный диагноз — ключ к выбору правильного лечения.
Как лечится аденомиоз?
Лечение аденомиоза частично зависит от ваших симптомов, их тяжести и от того, закончили ли вы деторождение. Легкие симптомы можно лечить с помощью безрецептурных обезболивающих и использования грелки для облегчения судорог.
Противовоспалительные препараты . Ваш врач может назначить нестероидные противовоспалительные препараты (НПВП) для облегчения легкой боли, связанной с аденомиозом.НПВП обычно начинают принимать за один-два дня до начала менструации и продолжают принимать в течение первых нескольких дней менструации.
Гормональная терапия . Симптомы, такие как обильные или болезненные месячные, можно контролировать с помощью гормональной терапии, такой как левоноргестрел-высвобождающая ВМС (которая вводится в матку), ингибиторы ароматазы и аналоги ГнРГ.
Эмболизация маточной артерии. В этой минимально инвазивной процедуре, которая обычно используется для уменьшения миомы, крошечные частицы используются для блокировки кровеносных сосудов, обеспечивающих приток крови к аденомиозу.Частицы направляются через крошечную трубку, вставленную радиологом в бедренную артерию пациента. При прекращении кровоснабжения аденомиоз сокращается.
Абляция эндометрия. Эта малоинвазивная процедура разрушает слизистую оболочку матки. Было обнаружено, что абляция эндометрия эффективна для облегчения симптомов у некоторых пациентов, когда аденомиоз не проник глубоко в мышечную стенку матки.
Вызывает ли аденомиоз бесплодие?
Поскольку многие женщины с аденомиозом также страдают эндометриозом, трудно точно сказать, какую роль аденомиоз может играть в проблемах с фертильностью.Однако некоторые исследования показали, что аденомиоз может способствовать бесплодию.
Можно ли вылечить аденомиоз?
Единственным окончательным лекарством от аденомиоза является гистерэктомия или удаление матки. Это лечение часто выбирают женщины со значительными симптомами.
Аденомиома — обзор | Темы ScienceDirect
Диагностические критерии
Гистологические признаки
Эндоцервикальная аденомиома — это классическая хорошо разграниченная двухфазная опухоль с железами, расположенными в строме, состоящей преимущественно из гладких мышц, расположенных в пучках.Железы, выстланные доброкачественным муцинозным эпителием эндоцервикального типа, имеют кистозную или неправильную форму и демонстрируют несколько дольчатый характер роста. Более крупные железы могут иметь вид коротких папиллярных складок. Могут присутствовать поверхностная плоскоклеточная, эндометриоидная и трубная метаплазия. Строма обычно лишена десмопластической реакции (рис. 15.17A и B).
Сообщалось о необычных особенностях, связанных с доброкачественной эндоцервикальной аденомиомой, включая стромальную реакцию в форме (1) гистиоцитарной и гигантоклеточной реакции в ответ на разрыв фокальной железы и экстравазации муцина, (2) аденофибромоподобный характер роста с выраженным сосочковые выступы, а также (3) симпластоподобная строма с причудливыми ядрами и многоядерными клетками. 104 Плоская интраэпителиальная неоплазия очаговой поверхности и стромальная жировая ткань также наблюдались в редких случаях. 104
Наличие выраженной архитектурной сложности желез, очаговой цитологической атипии, плоскоклеточных морул и очагового некроза может поставить диагноз атипичной полиповидной аденомиомы, когда признаков недостаточно для качественного или количественного диагноза аденосаркомы. Мы рекомендуем последующее наблюдение с наблюдением за пациентом на предмет повторного роста полипа, когда мы сталкиваемся с необычными поражениями любого типа.
Иммуногистохимия
Иммуногистохимия не имеет большого значения при диагностике классической аденомиомы, хотя в сложных случаях иммуноокрашивание может быть дополнительным диагностическим средством. Миоматозный стромальный компонент можно выделить с помощью актина гладких мышц, десмина и H-кальдесмона. Кейси и др. сообщили о диффузной положительности ER, CK7 и PAX8, положительности для карциноэмбрионального антигена (CEA; апикальный), а также об отрицательности для MUC6, согласующейся с доброкачественным эндоцервикальным иммунофенотипом в железистых компонентах эндоцервикальной аденомиомы, что отличает их от гистологических имитаций, таких как минимальные — аденокарцинома с отклонениями и лобулярная эндоцервикальная железистая гиперплазия (LEGH), которые обычно имеют иммунофенотип желудка. 101-104 Иммунореактивность для ER была резюмирована в последующем описании случая Takeda et al., Хотя очаговая реактивность для MUC6 наблюдалась в этом исследовании. 106 Более того, аденомиома демонстрирует либо сохранение, либо гетерогенную экспрессию PAX2, что помогает отличить ее от аденокарциномы с минимальным отклонением, при которой экспрессия PAX2 часто теряется. 107
Дифференциальный диагноз
Когда аденомиома шейки матки представляет собой образование на фреске, основным дифференциальным диагнозом является аденокарцинома с минимальным отклонением (злокачественная аденома), поскольку обе опухоли могут иметь железы неправильной формы, выстланные мягким слизистым эпителием.Различие проводится на основе четко очерченной природы и частого лобулярного железистого расположения аденомиомы, что редко встречается при злокачественной аденоме, поскольку последняя обычно представляет собой нечеткое поражение со случайным инфильтративным ростом желез. Другие гистологические особенности, которые помогли дифференцировать эти две сущности, включают наличие стромальной десмоплазии, стромальной цитологической атипии и митотической активности, которые выявляются, по крайней мере, очагово во всех случаях злокачественной аденомы, но не присутствуют в аденомиоме.В образцах кюретажа четко очерченная природа аденомиомы шейки матки не может быть хорошо оценена, а комбинация желез и гладкомышечной стромы может указывать на инвазию, если человек не осознает возможность аденомиомы. 99-103
Первичные злокачественные опухоли, которые следует исключить, — это аденосаркома Мюллера, которая, в отличие от аденомиомы, содержит клеточную строму с перигландулярной конденсацией и минимальной дифференцировкой гладких мышц, и часто демонстрирует ядерную атипию, митозы и внутрижелезистые папиллярные выросты в аденомиоме. 105
Доброкачественные псевдоопухолевые поражения желез также необходимо отличать от эндоцервикальной аденомиомы. Подобно аденомиоме, ламинарная эндоцервикальная железистая гиперплазия (LEGH) может проявляться у женщин в пременопаузе в виде хорошо разграниченного поражения и дольчатого разрастания желез. 105 В LEGH, однако, отсутствует миоматозная строма, и железы выстланы столбчатым муцинозным эпителием с эозинофильным зернистым видом и иммунофенотипом желудка (положительным для HIK1083, который выделяет слизистые клетки желудка, и M-CGMC- 1, окрашивающий муцин пилорического типа). 108 Доброкачественный эндоцервикальный полип может также содержать пучки гладких мышц, но они часто являются второстепенными компонентами поражения, и их не следует путать с аденомиомой. 104 Эндоцервикоз может вызывать необходимость в рассмотрении эндоцервикальной аденомиомы, но первая не имеет миоматозной стромы и менее четко очерчена. Мезонефрическая гиперплазия шейки матки может иметь дольчатую архитектуру. В литературе сообщалось о поражении шейки матки, названном мезонефрической аденомиомой, с железами мезонефрического типа, состоящими из CD10-положительного ER-отрицательного простого кубовидного эпителия, расположенного в строме, содержащей большое количество гладких мышц. 104
Исход и лечение
Эндоцервикальные аденомиомы обычно лечат путем местного иссечения или простой полипэктомии. Остаточная опухоль после полипэктомии может быть обнаружена при гистерэктомии, и в редких случаях сообщалось о рецидиве через 3 года после полипэктомии. 99
Аденомиоматозный полип матки у пациентки, принимающей тамоксифен | Японский журнал клинической онкологии
Аннотация
Мы сообщаем о случае аденомиоматозного полипа, который развился во время лечения тамоксифеном от рака груди.63-летняя японка поступила с жалобами на атипичное генитальное кровотечение. Девятью месяцами ранее ей была сделана модифицированная радикальная мастэктомия по поводу рака правой груди, I стадии, положительной по рецепторам эстрогена (T1N0M0). Сразу после операции было начато введение тамоксифена в дозе 20 мг / сут. При обследовании органов малого таза после приема тамоксифена в течение 9 месяцев выяснилось, что матка увеличена до размеров кулака. Трансвагинальное ультразвуковое исследование и магнитно-резонансная томография выявили большую твердую массу с множеством кистозных областей в полости матки.Патологический диагноз опухоли после тотальной гистерэктомии — типичный аденомиоматозный полип. Считалось, что он развился во время приема тамоксифена.
Введение
Тамоксифен — нестероидный препарат, обладающий свойствами агониста и антагониста эстрогена (1). Его свойства антагониста эстрогена квалифицировали тамоксифен как важный метод лечения пациентов с раком груди, особенно тех, опухоли которых положительны на рецепторы эстрогена.Fisher и его коллеги (2) недавно рекомендовали, чтобы все пациенты с низким риском рака груди получали адъювантную терапию, и большое количество женщин в пременопаузе и постменопаузе получали тамоксифен в течение 3-5 лет. Потенциальные побочные эффекты препарата включают развитие рака эндометрия (3), полипов эндометрия (4-8), аденомиоза (9), лейомиомы (10,11) и кист яичников (12,13).
Аденомиоматозный полип (полиповидная аденомиома) эндометрия — это редкое полиповидное поражение, при котором стромальный компонент в значительной степени или исключительно состоит из гладких мышц (14).В этом отчете описан случай аденомиоматозного полипа, связанный с лечением рака груди тамоксифеном.
История болезни
63-летняя японка, беременность 8, параграф 2, поступила с жалобами на атипичное генитальное кровотечение. Девятью месяцами ранее она перенесла модифицированную радикальную мастэктомию правой груди по поводу эстроген-положительной стадии I (T1N0M0) болезни. Сразу после операции начали прием тамоксифена в дозе 20 мг / сут.До введения тамоксифена в анамнезе не было увеличения матки.
При гинекологическом осмотре после приема тамоксифена в течение 9 месяцев матка пациентки увеличилась до размеров кулака. Трансвагинальное ультразвуковое исследование выявило большую твердую массу (60 × 50 × 40 мм) с множественными кистозными участками в полости матки (рис. 1). Магнитно-резонансная томография (МРТ) выявила хорошо очерченную круглую опухоль (60 × 50 мм) в полости матки. МРТ опухоли продемонстрировала интенсивность сигнала от средней до высокой на T2-взвешенных изображениях и от низкой до высокой интенсивности сигнала на T1-взвешенных изображениях (рис.2). Зона сочленения сохранилась практически полностью. Области с высокой интенсивностью сигнала на T1-взвешенных изображениях были усилены увеличением контраста. Биопсия эндометрия не выявила признаков злокачественности.
Рисунок 1
Трансвагинальное ультразвуковое исследование показало большую твердую массу с множеством кистозных областей (60 x 50 x 40 мм) в полости матки.
Рисунок 1
Трансвагинальное ультразвуковое исследование показало большую твердую массу с множеством кистозных областей (60 x 50 x 40 мм) в полости матки.
Рисунок 2
МРТ таза. На T1-взвешенном изображении аксиального среза выявлена хорошо очерченная круглая опухоль (60 × 50 мм) в полости матки. МРТ опухоли показала интенсивность сигнала от низкой до высокой на T1-взвешенных изображениях. Зона сочленения сохранилась практически полностью.
Рисунок 2
Результаты МРТ таза. На T1-взвешенном изображении аксиального среза выявлена хорошо очерченная круглая опухоль (60 × 50 мм) в полости матки.МРТ опухоли показала интенсивность сигнала от низкой до высокой на T1-взвешенных изображениях. Зона сочленения сохранилась практически полностью.
Стандартные лабораторные данные были в пределах нормы. Уровни CA-125, CA 72-4 и CA 19-9 составляли 180 Ед / мл, 31,8 Ед / мл и 7,2 Ед / мл соответственно. Эти данные убедительно свидетельствуют о доброкачественной подслизистой опухоли с кистозной дегенерацией, такой как дегенерированная лейомиома. Тотальная гистерэктомия и двусторонняя сальпингоофорэктомия были выполнены в связи с постоянным кровотечением и для исключения злокачественного новообразования.Послеоперационное течение пациента протекало без осложнений.
При патологическом исследовании установлено, что полиповидная опухоль возникла из верхнего сегмента тела матки. Иссеченные поражения представляли собой бледные, эластичные, четко очерченные полиповидные образования с гладкой поверхностью (рис. 3). Гистологическое исследование показало, что опухоль состоит из желез эндометрия с примесью гладкомышечных клеток. Часто возникала кистозная дилатация желез эндометрия (рис. 4). Ни железистый эпителий, ни стромальные клетки не проявляли атипии.Плоской метаплазии железистого эпителия не наблюдалось. Патологический диагноз — аденомиоматозный полип матки.
Обсуждение
Тамоксифен эффективно блокирует действие эстрогенов на ткань-мишень и поэтому используется в качестве адъювантного лекарства у пациентов, у которых рак молочной железы является положительным по рецепторам эстрогена. Считается, что это антигормональное лечение выбора для пациентов с запущенным раком, а также для пациентов с низким риском (2).Тамоксифен проявляет свойства как агониста, так и антагониста эстрогена (1). Хотя тамоксифен является антагонистом эстрогена в груди (15), он является агонистом эстрогена в нижних отделах половых путей (16,17). Тамоксифен оказывает эстрогенное действие на миометрий, и сообщалось, что во время его приема развиваются лейомиомы (10,11). В описанных случаях размер миомы быстро увеличивался после начала приема тамоксифена. Тамоксифен также оказывает эстрогенное действие на эндометрий, и сообщалось о большом количестве случаев развития рака эндометрия во время терапии тамоксифеном (3).Полипы эндометрия также наблюдались во время приема тамоксифена у женщин в постменопаузе (4-8). Кроме того, Cohen et al. (9) сообщил о нескольких случаях аденомиоза у пациентов в постменопаузе, получавших тамоксифен. Они сообщили, что частота аденомиоза увеличивалась при приеме тамоксифена.
Рисунок 3
Аденомиоматозный полип, возникающий в верхнем сегменте тела матки. Повреждение представляло собой бледное, эластичное, хорошо очерченное полиповидное образование с гладкой поверхностью.
Рисунок 3
Аденомиоматозный полип, возникающий в верхнем сегменте тела матки. Повреждение представляло собой бледное, эластичное, хорошо очерченное полиповидное образование с гладкой поверхностью.
Рисунок 4
Гистологические данные области низкой интенсивности сигнала на T1-взвешенных изображениях. Кистозная дилатация желез эндометрия часто наблюдалась в пределах аденомиоматозного полипа.
Рисунок 4
Гистологические данные области низкой интенсивности сигнала на T1-взвешенных изображениях.Кистозная дилатация желез эндометрия часто наблюдалась в пределах аденомиоматозного полипа.
Аденомиоматозные полипы встречаются редко, всего 1,3% у пациентов с полипами эндометрия (18). Хертиг и Гор (19) сообщили, что поражения обычно обнаруживаются у бесплодных молодых пациентов. Большинство пациенток в нашем предыдущем исследовании находились в пременопаузе (14). Аденомиоматозные полипы состоят из желез эндометрия, смешанных с гладкомышечными клетками, которые имеют тенденцию к инволюции после менопаузы из-за снижения выработки эстрогенов.Cohen et al. (9) сообщил о случае постменопаузального аденомиоматозного полипа, развившегося во время приема тамоксифена. В данном случае аденомиоматозный полип, как полагают, возник после менопаузы в результате введения тамоксифена.
Hulka and Hall (7) сообщили о семи случаях полипа эндометрия, во всех из которых при ультразвуковом исследовании были обнаружены небольшие кистозные пространства в полипе. Наши результаты ультразвукового исследования соответствовали их результатам. В нашем случае МРТ также была полезна для оценки аномалий эндометрия.Области низкой интенсивности сигнала на T1-взвешенных изображениях могут отражать множественное кистозное расширение железы эндометрия в аденомиоматозном полипе.
Сокращение
МРТ
Магнитно-резонансная томография.
Сокращение
Список литературы
1,,.Фармакодинамические и биологические эффекты антиэстрогенов в различных моделях
,J Steroid Biochem
,1988
, vol.31
(стр.613
—43
) 2,,,,, и др.Рандомизированное клиническое испытание по оценке тамоксифена в лечении пациентов с раком молочной железы без лимфоузлов и опухолями, положительными по рецепторам эстрогена.
,N Engl J Med
,1989
, vol.320
(стр.479
—84
) 3,,.Гинекологические опухоли у женщин, получавших тамоксифен, с раком груди
,Obstet Gynecol
,1993
, vol.82
(стр.165
—9
) 4,,,,,.Изменения эндометрия у пациенток с раком молочной железы в постменопаузе, получающих тамоксифен
,Obstet Gynecol
,1993
, vol.81
(стр.660
—4
) 5,,,,,.Постменопаузальное кровотечение из необычных полипов эндометрия у женщин, получающих хроническую терапию тамоксифеном
,Obstet Gynecol
,1992
, vol.79
(стр.111
—6
) 6,,,,.Влияние тамоксифена на эндометрий
,Breast Cancer Res Treat
,1993
, vol.26
(стр.101
—5
) 7,.Аномалии эндометрия, связанные с терапией тамоксифеном при раке груди: сонографическая и патологическая корреляция
,Am J Roentgenol
,1993
, vol.160
(стр.809
—12
) 8,,,,, и др.Влияние тамоксифена на матку и яичники у женщин в постменопаузе в рандомизированном исследовании профилактики рака груди
,Ланцет
,1994
, vol.343
(стр.1318
—21
) 9,,,,, и др.Аденомиоз у пациенток с раком молочной железы в постменопаузе, получавших тамокс-ифен: новое явление?
,Gynecol Oncol
,1995
, т.58
(стр.86
—91
) 10,,,.Быстрый рост лейомиомы у пациента, получающего тамоксифен
,Am J Obstet Gynecol
,1992
, vol.166
(стр.167
—8
) 11,,,,, и др.Лейомиомы у пациентов, получающих тамоксифен
,Clin Exp Obstet Gynecol
,1994
, vol.21
(стр.94
—8
) 12,,,.Перекрут яичника у женщины в пременопаузе, получавшей тамоксифен от рака груди
,Fertil Steril
,1993
, vol.59
(стр.459
—60
) 13,,,,.Кисты яичников у женщин с раком груди в пременопаузе и постменопаузе, получавших тамоксифен
,Am J Obstet Gynecol
,1996
, vol.174
(стр.141
—4
) 14,,.Аденомиоматозный полип матки
,Int J Gynecol Obstet
,1995
, vol.48
(стр.319
—21
) 15.Контролируемое испытание тамоксифена в качестве единственного адъюванта при лечении рака груди на ранних стадиях: анализ через шесть лет, проведенный организацией по исследованию адъювантов Nolvadex
,Cancer
,1985
, vol.1
(стр.836
—9
) 16,,,,.Эстрогеноподобное действие тамоксифена на эпителий влагалища у больных раком груди
,Онкология
,1981
, vol.38
(стр.281
—8
) 17,,,.Тамоксифен увеличивает количество эстроген-связывающих эквивалентов в плазме и оказывает агонистическое действие на эстрадиол на гистологически нормальный эндометрий в пременопаузе и постменопаузе
,Fertil Steril
,1992
, vol.57
(стр.320
—7
) 18,.Полипы эндометрия
,Obstet Gynecol
,1956
, vol.8
стр.40
19,. ,Опухоли женских половых органов. Часть 2-Дополнение. Опухоли вульвы, влагалища и матки. Атлас патологии опухолей
,1968
Вашингтон, округ Колумбия
Институт патологии вооруженных сил
стр.322
Рак эндометрия — Американский семейный врач
1. Parker SL, Тонг Т, Болден С, Wingo PA.Статистика рака 1997. CA Cancer J Clin . 1997; 47: 5–27 [Опечатка опубликована в CA Cancer J Clin 1997; 47: 68] …
2. Берек Дж. С., Хакер Н. Ф., ред. Практическая гинекологическая онкология. 2-е изд. Балтимор: Уильямс и Уилкинс, 1994: 285–326.
3. Баракат р. Современные проблемы лечения рака эндометрия. CA Cancer J Clin . 1998. 48: 299–314.
4. Ференци А., Гельфанд М.М., Циприс Ф. Цитодинамика гиперплазии и карциномы эндометрия: обзор. Энн Патол . 1983; 3: 189–202.
5. Курман Р.Ю., Камински П.Ф., Норрис HJ. Поведение гиперплазии эндометрия: долгосрочное исследование «нелеченой» гиперплазии у 170 пациентов. Рак . 1985; 56: 403–12.
6. Ференци Р.Дж., Гельфанд М. Биологическое значение цитологической атипии при гиперплазии эндометрия, леченной прогестогенами. Ам Дж. Обстет Гинекол . 1989; 160: 126–31.
7. Курман Р.Дж., Норрис Х.Дж.Карцинома эндометрия. В кн .: Курман Р.Ж., под ред. Патология Блаустейна женских половых путей. 3-е изд. Нью-Йорк: Springer-Verlag, 1987: 352.
8. Пома П.А. Рак эндометрия: уделять больше внимания профилактике. Пациентка . 1997; 22: 39–43.
9. Parazzini F, Ла Веккья C, Боччолон L, Франчески С. Эпидемиология рака эндометрия. Гинеколь Онкол . 1991; 41: 1–16.
10. Баракат р.Тамоксифен и неоплазия эндометрия. Clin Obstet Gynecol . 1996; 39: 629–40.
11. Mack TM, Щука MC, Хендерсон Б.Е., Пфеффер Р.И., Геркинс VR, Артур М, и другие. Эстрогены и рак эндометрия в пенсионном сообществе. N Engl J Med . 1976; 294: 1262–7.
12. Грейди Д, Гебрецадик Т, Kerlikowske K, Эрнстер V, Петитти Д. Заместительная гормональная терапия и риск рака эндометрия: метаанализ. Акушерский гинекол . 1995; 85: 304–13.
13. Гамбрелл Р. Д. Мл. Стратегии снижения заболеваемости раком эндометрия у женщин в постменопаузе. Ам Дж. Обстет Гинекол . 1997; 177: 1196–207.
14. Группа разработчиков исследования PEPI. Влияние заместительной гормональной терапии на гистологию эндометрия у женщин в постменопаузе: исследование постменопаузальных эстроген / прогестиновых вмешательств (PEPI). ЯМА . 1996. 275: 370–5.
15.Ng AB, Рейган Дж. В., Хавличек С, Венц Б.В. Значение клеток эндометрия в обнаружении рака эндометрия и его предшественников. Акта Цитол . 1974; 18: 356–61.
16. Джонс М.В., Курман Р.Дж. Новые способы лечения гиперплазии эндометрия. Contemp Ob Gyn . 1990; 35: 36–46.
17. Американский колледж акушеров и гинекологов. Карцинома эндометрия. Технический бюллетень № 162. Вашингтон Д.C .: Американский колледж акушеров и гинекологов, 1991.
18. Коэн CJ, Гусберг С.Б., Коффлер Д. Гистологический скрининг на рак эндометрия. Гинеколь Онкол . 1974; 2: 279–86.
19. Creasman WT, Вид JC Jr. Методы скрининга рака эндометрия. Рак . 1976; 38 (1 доп.): 436–40.
20. Уолтерс Д., Робинсон Д, Парк ЖК, Patow WE. Диагностический амбулаторный аспирационный кюретаж. Акушерский гинекол . 1975; 46: 160–4.
21. Лангер Р.Д., Пирс Джей Джей, О’Ханлан К.А., Джонсон С.Р., Эспеланд, Массачусетс, Трабал Ю.Ф., и другие. Трансвагинальное ультразвуковое исследование в сравнении с биопсией эндометрия для выявления заболевания эндометрия: исследование вмешательств эстрогена / прогестина в постменопаузе. N Engl J Med . 1997; 337: 1792–8.
22. Van den Bosch T, Вандендал А, Ван Шуброк Д., Вранц П.А., Ломбард CJ.Сочетание вагинального ультразвукового исследования и лабораторного исследования эндометрия в диагностике заболеваний эндометрия у женщин в постменопаузе. Акушерский гинекол . 1995; 85: 349–52.
23. Родригес GC, Якуб Н, Король МЕНЯ. Сравнение устройства Pipelle и аспиратора Vabra по результатам измерения денудации эндометрия в образцах гистерэктомии: устройство Pipelle отбирает значительно меньше поверхности эндометрия, чем аспиратор Vabra. Ам Дж. Обстет Гинекол .1993. 168 (pt 1): 55–9.
24. Стовалл Т.Г., Линг ФВ, Morgan PL. Проспективное рандомизированное сравнение устройства для отбора проб эндометрия Pipelle с кюреткой Novak. Ам Дж. Обстет Гинекол . 1991; 165 (часть 1): 1287–90.
25. Блюменфельд М.Л., Тернер Л.П. Роль трансвагинальной сонографии в оценке гиперплазии эндометрия и рака. Clin Obstet Gynecol . 1996; 39: 641–55.
26. Карлссон Б., Гранберг С, Викланд М, Илостало П, Торвид К, Марсал К, и другие.Трансвагинальное ультразвуковое исследование эндометрия у женщин с кровотечением в постменопаузе: многоцентровое исследование Nordic. Ам Дж. Обстет Гинекол . 1995; 172: 1488–94.
27. Lerner JP, Тимор-Трич ИП, Монтеагудо А. Использование трансвагинальной сонографии при оценке гиперплазии и карциномы эндометрия. Наблюдение за акушерством и гинекологом . 1996; 51: 718–25.
28. Международная федерация гинекологии и акушерства. Годовой отчет о результатах лечения гинекологического рака. Int J Gynecol Obstet . 1989; 28: 189–90.
29. Подрац KC, О’Брайен ПК, Малкасян Г.Д. мл., Деккер Д.Г., Джеффрис Дж. А., Эдмонсон Дж. Эффекты прогестагентов при лечении рака эндометрия. Акушерский гинекол . 1985; 66: 106–10.
30. Пивер МС, Барлоу Дж. Дж., Лурайн-младший, Blumenson LE. Медроксипрогестерона ацетат (Депо-Провера) против гидроксипрогестерона капроата (Делалутин) у женщин с метастатической аденокарциномой эндометрия. Рак . 1980; 45: 268–72.
31. Moore TD, Филипс PH, Неренстон SR, Cheson BD. Системное лечение запущенной и рецидивирующей карциномы эндометрия: текущее состояние и направления на будущее. Дж Клин Онкол . 1991; 9: 1071–88.
32. Randall TC, Курман Р.Дж. Прогестинотерапия атипичной гиперплазии и высокодифференцированной карциномы эндометрия у женщин в возрасте до 40 лет. Obstet Gynecol .1997; 90: 434–40.
33. McGonigle KF. Как прогестины снижают риск рака эндометрия у пользователей ФЗТ. Contemp Ob Gyn . 1997. 42: 96–108.
Практический подход к диагностике смешанных эпителиальных и мезенхимальных опухолей матки
По определению ВОЗ аденосаркома — это смешанная эпителиально-мезенхимальная опухоль, в которой эпителиальный компонент является доброкачественным или атипичным, а стромальный компонент является злокачественным низкоуровневым. ‘. 1 Аденосаркомы встречаются редко и являются третьим по распространенности подтипом саркомы матки после лейомиосаркомы и стромальной саркомы эндометрия низкой степени злокачественности.В недавнем популяционном исследовании из Норвегии аденосаркомы составляли 5,5% сарком матки. 33 Аденосаркома обычно рассматривается как новообразование с низким потенциалом злокачественности, способное к локальному рецидиву и иногда к отдаленным метастазам. Тело матки является наиболее частым местом в женских половых путях, но эти новообразования также возникают в шейке матки, яичниках или влагалище или, реже, в брюшине. 34, 35, 36, 37
Клинические особенности
Аденосаркома матки встречается во всех возрастных группах, но чаще всего встречается у женщин после менопаузы.В самой большой серии сообщений опухоли возникли у пациентов в возрасте 14–89 лет (в среднем 58 лет). 35 Наиболее частым симптомом является аномальное вагинальное кровотечение, но у некоторых пациентов наблюдаются боли в области таза, образование в брюшной полости или выделения из влагалища. У некоторых пациентов в анамнезе могут быть рецидивирующие полипы эндометрия или шейки матки. Сообщалось о связи с тамоксифеном, гиперэстрогенизмом и предшествующим облучением органов малого таза. 38 Однако это могут быть случайные ассоциации, и доказанных этиологических факторов нет.
Патологические особенности
Аденосаркома чаще всего возникает из эндометрия, иногда поражая нижний сегмент матки, но некоторые могут возникать в шейке матки или миометрии в результате аденомиоза. 34, 35, 36, 37, 39 Полость матки обычно заполнена и расширена полиповидной дольчатой, губчатой или эластичной массой, которая может выступать через зев шейки матки. На поверхности разреза могут быть кисты или щели различного размера (рис. 6). Часто наблюдается очаговое кровотечение и некроз.Некоторые новообразования образуют множественные полипы.
Рисунок 6Макро-микрофотография аденосаркомы с полиповидным дольчатым поражением, содержащим щели (любезно предоставлено доктором Робином Янгом, Массачусетская больница общего профиля, Бостон, Массачусетс, США).
Гистологически смешанный характер опухоли иллюстрируется наличием как эпителиальных, так и стромальных элементов, причем последние преобладают. При малом увеличении опухоль часто имеет филлодоподобную (листообразную или булавовидную) архитектуру (рис. 7).Эпителиальные элементы обычно состоят из желез, которые могут быть расширенными или щелевидными, иметь вид филлодий, выстланных кубовидными или низко столбчатыми клетками. В большинстве случаев эпителий эндометриоидный и напоминает пролиферативный эндометрий, хотя также может наблюдаться мерцательный, муцинозный и плоский эпителий. В редких случаях эпителиальный компонент проявляет железистую сложность, напоминающую атипичную гиперплазию / интраэпителиальную неоплазию или карциному эндометрия. Последний обычно представляет собой эндометриоидный рак низкой степени злокачественности. 28 Стромальный компонент, который обычно низкосортный, состоит из веретенообразных и / или круглых клеток со скудной цитоплазмой, но редко может быть высокосортным. Характерны внутрижелезистые выступы стромы и способ, которым стромальные клетки, которые часто напоминают стромальные клетки эндометрия, концентрируются вокруг или под железистыми элементами («перигландулярные манжеты») (рис. 8). «Наручники» могут быть очень тонкими (и, таким образом, упускать из виду), но именно там обычно обнаруживаются ядерная атипия и митотическая активность (Рисунок 9).Хотя часто наблюдается митотическая скорость ≥2 на 10 мощных полей (HPF), некоторые опухоли имеют более низкую митотическую скорость и должны быть диагностированы как аденосаркома, если опухоль имеет характерные вышеупомянутые особенности, отраженные в классификации ВОЗ 2014 года. 1
Рисунок 7Мюллерова аденосаркома низкой степени злокачественности. Обратите внимание на ярко выраженную филлодоподобную архитектуру, связанную с перигландулярной стромальной конденсацией.
Рисунок 8Мюллерова аденосаркома низкой степени злокачественности.Характерны полиповидные выступы внутри просвета.
Рисунок 9Мюллерова аденосаркома низкой степени злокачественности. Строма вокруг желез гиперклеточная, клетки имеют повышенное ядерное и цитоплазматическое соотношение, показывают цитологическую атипию и повышенную митотическую активность.
Большинство аденосарком содержат исключительно гомологичные мезенхимальные элементы, включая гладкие мышцы с веретеновидной или эпителиоидной морфологией. 38 Элементы, похожие на половой шнур, состоящие из гнезд, тяжей, твердых или полых канальцев и идентичные тем, которые наблюдаются в стромальных новообразованиях эндометрия, могут присутствовать в мезенхимальном компоненте; они могут быть положительными на маркеры полового шнура, такие как ингибин и кальретинин (рис. 10). 40 Элементы, похожие на половой шнур, могут содержать обильную эозинофильную или пенистую цитоплазму. В редких случаях внутри аденосаркомы наблюдается чрезмерное разрастание элементов, подобных половому шнуру. 41, 42 Примерно 25% этих опухолей могут содержать гетерологичные стромальные элементы, чаще всего рабдомиобласты и хрящи эмбрионального типа и редко липобласты. 40 Гетерологичные элементы обычно представляют собой второстепенный компонент стромы, но иногда широко распространены. Сообщалось о обширной гиалинизации, миксоидных изменениях или децидуализации. 41
Рис. 10Мюллерова аденосаркома низкой степени злокачественности с элементами, подобными половому шнуру. Гнезда эпителиоподобных клеток присутствуют в неопластической строме низкой степени злокачественности ( a ). Эти клетки строго положительны по ингибину (b ).
Большинство аденосарком ограничены эндометрием или слизистой оболочкой шейки матки. Примерно 15% проникают в миометрий, обычно во внутреннюю половину, или в строму шейки матки. Миоинвазивный компонент обычно состоит как из эпителиальных, так и из стромальных элементов, но он может состоять только из саркомы, которая может быть более высокой степени.Глубокая инвазия гораздо чаще встречается при саркоматозном разрастании (см. Ниже). Сосудистая инвазия встречается редко, но иногда, особенно при глубокой инвазии миометрия или саркоматозном разрастании.
Аденосаркома с разрастанием саркомы
Саркоматозное разрастание определяется как наличие чистой саркомы (без эпителиальных элементов), составляющей> 25% опухоли. 1 Саркома, как правило, высокой степени злокачественности и может состоять из рабдомиосаркомы или недифференцированной саркомы (рис. 11).В редких случаях саркома при чрезмерном саркоме может быть низкой степени злокачественности. Саркоматозное разрастание обычно связано с глубокой инвазией миометрия и сосудов и является наиболее важным прогностическим фактором. 42
Рисунок 11Мюллерова аденосаркома с саркоматозным разрастанием. Компонент высокой степени злокачественности напоминает недифференцированную саркому.
Дополнительные исследования
Стромальный компонент низкой степени злокачественности обычно экспрессирует рецептор эстрогена (ER), рецептор прогестерона (PR), CD10, WT1 и актин гладкой мускулатуры, а также имеет низкий индекс пролиферации MIB1. 43 Реже встречаются рецепторы андрогенов, AE1 / AE3, десмин и кальретинин положительные. В областях чрезмерного роста саркомы (высокой степени) мезенхимальный компонент демонстрирует более высокий индекс пролиферации MIB1, и обычно наблюдается потеря экспрессии ER, PR и CD10, иммунофенотип аналогичен недифференцированной саркоме матки. Области рабдомиосаркомы экспрессируют десмин и маркеры скелетных мышц (миогенин и myoD1). Элементы, подобные половому шнуру, могут экспрессировать ингибин, кальретинин и другие маркеры полового шнура. 36
Недавнее исследование основных молекулярных событий в аденосаркоме с использованием секвенирования следующего поколения обнаружило амплификацию MDM2 и CDK4 со сверхэкспрессией белка в некоторых опухолях. Также были обнаружены изменения в пути PIK3CA / AKT / PTEN, но мутации Tp53 и были необычными. Мутации ATRX и амплификация MYBL1 наблюдались только в опухолях с чрезмерным саркоматозным разрастанием. 44
Прогноз
Пациенты с аденосаркомой имеют, как правило, хороший прогноз, если опухоль не демонстрирует глубокую инвазию миометрия или не имеет саркоматозного разрастания.Рецидивы, которые возникают у 20–30% пациентов, обычно ограничиваются влагалищем, тазом или брюшной полостью. 35 Они чаще всего состоят исключительно из саркомы, которая обычно, но не всегда, более высокой степени, чем мезенхимальный компонент исходного новообразования. В некоторых случаях рецидив бывает двухфазным. Отдаленные метастазы, которые возникают нечасто, почти всегда представляют собой чистую саркому. Возможны поздние рецидивы; следовательно, необходимо долгосрочное наблюдение.
Стадия
Аденосаркомы имеют отдельную систему стадий, чем лейомиосаркомы и стромальные саркомы эндометрия. 45 Аденосаркомы I стадии ограничены маткой (тело и шейка матки) с подстадиями IA, IB и IC (опухоль ограничена эндометрием / эндоцервиксом без инвазии миометрия, меньше или равна половине инвазии миометрия, больше половины инвазии миометрия , соответственно). Некоторые мюллеровы аденосаркомы с необычным характером роста могут быть трудными для стадии, в частности, когда они связаны с аденомиозом или возникают в настенных аденомиомах. 39
Дифференциальный диагноз
Аденофиброма
Одной из основных проблем дифференциальной диагностики аденосаркомы является аденофиброма.Согласно определению ВОЗ 2003 года, аденосаркома отличалась от аденофибромы наличием митотического числа стромы 2 или более на 10 HPF, значительной клеточностью стромы с перигландулярными манжетами и более чем легкой ядерной атипией стромальных клеток. 46 Однако, как уже говорилось, эта степень митотической активности не всегда присутствует в аденосаркомах, и это отражено в Классификации ВОЗ 2014 года, где не дано митотическое отсечение, чтобы различать аденосаркому и аденофиброму. 1 Аденосаркома встречается гораздо чаще, чем аденофиброма, и существуют разногласия относительно существования аденофибромы. 36, 47 Уверенный диагноз аденофибромы не может быть поставлен на основании биопсии или полипэктомии, поскольку аденосаркома не может быть исключена, если вся опухоль не доступна для гистологического исследования. Используя эти строгие критерии, диагноз аденофибромы ставится очень редко, и с практической точки зрения этот диагноз не может быть поставлен на основе биоптата.Можно утверждать, что все аденофибромы на самом деле являются аденосаркомами низкой степени злокачественности или хорошо дифференцированными, поскольку даже при отсутствии митотической активности случаи могут повторяться или даже редко даже метастазировать. 47 Было предложено объединить аденофибромы и аденосаркомы в единую категорию неопластов, и термин «аденофиброма» был исключен. Хотя аденофиброма сохраняется в классификации ВОЗ 2014 г., этот диагноз следует ставить осторожно. 1
Недифференцированная саркома или плеоморфная рабдомиосаркома
При аденосаркоме с разрастанием саркомы большие области опухоли могут морфологически соответствовать недифференцированной саркоме или плеоморфной рабдомиосаркоме.Однако следует провести обширный отбор образцов, который может выявить области диагностики аденосаркомы.
Карциносаркома
В отличие от аденосаркомы низкой степени злокачественности, карциносаркома содержит явно злокачественные эпителиальные элементы в дополнение к саркоматозному компоненту. Стромальный компонент почти всех карциносарком имеет высокую степень злокачественности и гораздо более плеоморфен, чем в большинстве аденосарком, и не имеет перигландулярных манжет повышенной клеточности стромы, которые характерны для аденосарком.Редкие карциносаркомы имеют маломощную архитектуру, что повышает вероятность аденосаркомы; тем не менее, это обычно очаговая находка, и при исследовании с большим увеличением эпителий демонстрирует явные цитологические признаки злокачественного новообразования.
Полипы эндометрия и шейки матки
Редкие полипы шейки матки или эндометрия содержат участки, которые повышают вероятность аденосаркомы. 48 Особенности, которые частично совпадают с теми, которые наблюдаются при аденосаркоме, включают в себя основные находки (1) «филлодоподобную» архитектуру, (2) внутрижелезистые стромальные выступы и / или (3) повышенную клеточность, окружающую железы (рис. 12а).Некоторые из этих особенностей могут наблюдаться в связи с терапией тамоксифеном. О таких случаях лучше всего сообщать как о «полипах эндоцервикального канала или эндометрия с необычными характеристиками». Недавно было показано, что исход всегда без происшествий. 48 Некоторые полипы эндометрия могут иметь однородно клеточную строму и могут содержать большое количество гладких мышц (аденомиомтозный полип) или атипичные стромальные клетки с симпластическим внешним видом (рис. 12b). 49 Эти данные не имеют клинического значения и не должны приводить к ошибочному диагнозу аденосаркомы.
Рисунок 12Полип эндометрия с необычными чертами. Вокруг некоторых желез имеется повышенная клеточность, что придает отдаленное сходство с аденосаркомой ( a ). Обратите внимание на ядра симпластического типа в стромальном компоненте полипа эндометрия, которые не следует ошибочно интерпретировать как саркому низкой степени злокачественности ( b ).
Атипичная полиповидная аденомиома
У этой двухфазной опухоли отсутствует филлодоподобная архитектура и перигландулярная манжета, а в стромальном компоненте наблюдается дифференцировка гладких мышц или миофибробластов.Эпителиальные элементы обычно имеют большую архитектурную сложность, чем при аденосаркоме, а также очаги плоской дифференцировки в виде морул, которые иногда показывают центральный некроз. Кроме того, при малой мощности можно отметить неопределенно лобулярную архитектуру. 50
Стромальная саркома эндометрия низкой степени с железистой дифференцировкой
Стромальная саркома эндометрия низкой степени может иногда иметь эндометриоидную железистую дифференцировку и, таким образом, повышать дифференциацию аденосаркомы; 51 однако, стромальные саркомы эндометрия обладают проницаемостью, а не деструктивной инвазией миометрия, миоинвазивный компонент имеет более однородный вид, и в нем отсутствуют перигландулярные стромальные манжеты, филлодоподобная архитектура или выраженная эпителиальная мюллерова метаплазия. 52
Эмбриональная рабдомиосаркома
Особенности эмбриональной рабдомиосаркомы, которые могут частично совпадать с маллеровской аденосаркомой низкой степени злокачественности, включают обнаружение небольших синих клеток, которые концентрируются под поверхностным эпителием и вокруг желез, имитирующих перигландулярные манжеты, хрящи и хрящи плода. чаще встречается в шейке матки, чем в теле или других местах. 53, 54 Отличительные особенности включают цитологическую атипию высокой степени, а также митотическую активность и апоптоз в мелких клетках, чередование областей гипер- и гипоцеллюлярности и малочисленность мюллеровых желез, которые захватываются, а не являются частью новообразования и не проявляются. типичная филлодоподобная архитектура.Гипоцеллюлярные области часто бывают миксоидными или отечными и могут иметь скопления клеток с более обильной эозинофильной цитоплазмой, включая поперечные полосы. В отличие от аденосаркомы, эмбриональная рабдомиосаркома чаще встречается в шейке матки, чем в теле матки. Иногда присутствуют очаги, напоминающие альвеолярную рабдомиосаркому, или скопления плеоморфных клеток с многолепестковыми ядрами. 55 Видны гиалиновые глобулы. Обычно наблюдаются участки кровотечения с экстравазированными эритроцитами или некрозом.Окрашивание ядер с помощью маркеров скелетных мышц (миогенин и myoD1) помогает в диагностике, но обычно только небольшая часть ядер являются иммунореактивными. Десмин обычно положительный, но актин гладких мышц и h-кальдесмон обычно отрицательны. Рецепторы гормонов (ER и PR) обычно отрицательны, в отличие от типичных областей аденосаркомы. Следует отметить, что существует редкая связь между шейной эмбриональной рабдомиосаркомой, опухолью из клеток Сертоли-Лейдига, кистозной нефромой, зобом щитовидной железы, плевропульмональной бластомой и другими эмбриональными новообразованиями, и это вторично по отношению к основной соматической или зародышевой мутации DICER1 . 50, 51, 52, 53, 54, 55, 56, 57, 58, 59
Типы гиперплазии эндометрия
Гиперплазия эндометрия (ГЭ) — это термин, обозначающий чрезмерный рост или утолщение эндометрия, внутренней оболочки матки. Обычно считается, что это происходит из-за повышенного роста клеток в результате воздействия беспрепятственного эстрогена, который способствует росту клеток эндометриальных желез.
Кредит: Татьяна Шепелева / Shutterstock.com
Это связано с такими состояниями, как синдром поликистозных яичников (СПКЯ) или ожирение, при обоих из которых уровни эстрогена высоки.Это потенциально серьезный диагноз, потому что, когда клетки проявляют атипичные признаки, EH может быть предшественником или даже маркером наличия рака матки.
Типы EH
или кюретаж (соскабливание эндометрия ложкой) проводится для получения образца ткани для исследования под микроскопом. Тем не менее, многие случаи настоящего рака могут быть пропущены из-за неполного отбора проб, и только окончательное обследование матки после гистерэктомии (удаление матки) показывает наличие рака эндометрия.
Старая классификация ВОЗ (1994 г.)
- Простая гиперплазия:
- без атипии 66% — Увеличенное количество желез, но с нормальной железистой структурой
- с атипией 2% — скученные нерегулярные железы
- Сложная гиперплазия:
- без атипии 11% — Простая гиперплазия с наличием цитологической атипии
- с атипией 14% — Сложная гиперплазия с цитологической атипией.
Определение терминов
Simple EH характеризуется равномерным утолщением как клеток железы, так и стромы, в отличие от того, что наблюдается при нормальном цикле матки, но без чрезмерного выступа клеток железы и с округлой формой железы.
Комплекс EH, с другой стороны, характеризуется повышенной пролиферацией железистых клеток с меньшим вовлечением стромы, что приводит к скоплению желез. Сами железы бывают разных форм и размеров, с заметными и неправильными ветвлениями и почками.
В обоих этих случаях атипия может присутствовать или отсутствовать. Этот термин относится к аномально большому размеру ядра с плотным хроматином. Часто бывает трудно сказать, когда простая гиперплазия перестает быть простой, поэтому оказалось, что эта классификация далека от воспроизводимости.
В первоначальном исследовании (Курман и др.) Частота прогрессирования простой гиперплазии до рака эндометрия составляла 3%, 8% и 29% соответственно для сложных, простых атипичных и сложных атипичных ГГ.
Другая классификация, применявшаяся в Германии, разделила ГГ на кистозно-железистую гиперплазию и аденоматозную гиперплазию, причем последняя подразделялась на степени от I до III в зависимости от наличия скученности и атипичных изменений в ядре.
Классификация маттеров
Более поздние работы патологов и клиницистов привели к появлению третьей системы (Mutter et al), которая классифицирует EH следующим образом:
- Доброкачественная гиперплазия, соответствующая простой гиперплазии в более ранних классификациях
- Внутриэпителиальная неоплазия эндометрия (EIN), при которой железы тесно переполнены небольшой стромой, клетки имеют аномальный вид, поражение превышает 1 мм в диаметре и другие инвазивные характеристики отсутствуют.Другие подобные условия также должны быть исключены.
Преимуществами этой системы являются ее лучшая воспроизводимость и тесная взаимосвязь между EIN и сложной атипичной EH в более ранних системах в отношении точного прогнозирования риска развития рака. Эта система рекомендована несколькими экспертными организациями из-за ее прогностической ценности.
Пересмотренная классификация ВОЗ
Последняя классификация ВОЗ (2014 г.) пытается упростить диагностику при микроскопии с большей точностью и, как следствие, лучшим лечением.Также учитывается наличие EIN при высоком проценте атипичных EH. Это по-прежнему наиболее широко используемая классификация в мире. В нем всего две категории, а именно
.- Гиперплазия без атипии
- Атипичная гиперплазия или EIN
Клинические достижения, отраженные в этой классификации, включают отсутствие генетических изменений в EH без атипии, что является полностью доброкачественным состоянием и может быть полностью обращено вспять после удаления источника эстрогена и лечения пациента адекватными дозами прогестерона.Скорость развития рака в этой группе низкая, около 1-3%, и обычно сопровождает длительное воздействие эстрогена.
С другой стороны, атипичная EH связана с раковыми мутациями, такими как инактивация PAX2 и мутациями в генах PTEN , KRAS и CTNNB1 (β-катенин), с нестабильностью микросателлитов. Это связано, как уже упоминалось, с чрезвычайно высоким риском рака эндометрия — до 60%. Очевидно, что отношение к обоим типам совершенно разное.
Атипичная EH диагностируется, когда клетки содержат ядерные аномалии, которые характерны для злокачественной опухоли или вызывают подозрение на нее. К ним относятся:
- потеря полярности в ячейках
- потеря нормального развития между слоями клеток эндометрия
- очень изменчивые формы и размеры ячеек
- круглые, а не столбчатые ядра
- Большой диаметр ядра по сравнению с размером ячейки
- очень плотные ядра с крупными ядрышками и сгруппированным хромосомным материалом, а не равномерно распределенным
- высокоэозинофильная цитоплазма, которая часто привлекает внимание к аномальному скоплению клеток
Частота ГЭ без атипии составляет лишь около 5% у бессимптомных женщин в пременопаузе, в то время как атипичная гиперплазия встречается примерно у 1% в этой группе.ГЭ встречается примерно у 10% пациентов с аномальным маточным кровотечением.
Наиболее распространенной формой рака эндометрия является эндометриоидная карцинома, которая имеет те же факторы риска, что и EH. Обычно это конечный результат атипичной ГГ и составляет около 85% случаев рака эндометрия. Фактически, до 60 из каждых 100 женщин с атипичной ГГ уже имеют реальный рак эндометрия или разовьются в нем в течение нескольких лет, поэтому этот диагноз лучше всего лечить с помощью тотальной гистерэктомии с удалением всей матки и шейки матки.По этой причине чрезвычайно важно поставить точный диагноз в этом состоянии, чтобы обеспечить наилучшую форму лечения.
Дополнительная литература
Отчет о двух случаях и обзор литературы
- © 2017 Ассоциация клинических ученых, Inc.
- Бинара Асылбекова⇑,
- Эстер Елишаев и
- Рохит Бхаргава
- Отделение патологии женской больницы Маги Медицинского центра Университета Питтсбурга, Питтсбург, Пенсильвания, США
- Адресная корреспонденция к Бинаре Асылбековой М.Д., МОЗ; Отделение патологии женской больницы Маги Университета Питтсбурга Медицинский центр, 300 Halket Street, Питтсбург, Пенсильвания 15216, США; телефон: +1832382-1731; e-mail: басылбекова {ат} gmail.com
Аннотация
Необычные варианты эндометриоидной аденокарциномы эндометрия могут быть сложными с диагностической точки зрения и затруднять дифференциацию от их доброкачественных и злокачественных имитаторов. Здесь мы описываем сущность, которая была хорошо задокументирована в литературе, но об истинном исходе мало что известно из-за отсутствия исследований с большим количеством случаев.Диффузно инфильтративный или «подобный злокачественной аденоме» представляет собой необычный образец инвазии в эндометриоидную аденокарциному эндометрия, которую можно спутать с аденомиозом. К насколько нам известно, только 58 случаев (исключая эти 2 случая) были зарегистрированы на сегодняшний день в английской литературе.
Введение
Диффузно инфильтрирующая или «подобная аденоме злокачественная» форма инвазии при эндометриоидной аденокарциноме эндометрия. что можно спутать с аденомиозом.Здесь мы представляем два таких необычных случая, один из которых был недавно удален, а другой — 9 лет. последующих действий. Насколько нам известно, только 58 случаев (исключая эти 2 случая) были зарегистрированы на сегодняшний день на английском языке. литература.
История болезни
Корпус 1
58-летняя женщина с аденокарциномой эндометрия «2 стадии» в анамнезе, диагностированной во внешнем стационаре 9 лет назад, была обратился в нашу больницу из-за образования в малом тазу, которое, как считается, представляет рецидив.Ей была сделана полная абдоминальная гистерэктомия с двусторонняя сальпингоофорэктомия и адъювантное внешнее лучевое облучение и брахитерапия при первоначальном диагнозе. Девять лет спустя После операции она обратилась к врачу с болью в левой нижней конечности, потерей рефлекса надколенника, дальнейшее обследование показало левую поясничную мышцу размером 4,2 см. мышечная масса. Слайды ее образца гистерэктомии были доступны для просмотра. Чаще всего видны срезы тела матки. поверхностный эндометрий со сложной атипичной гиперплазией с более глубокими участками, показывающими банальные железы, вторгающиеся в миометрий без любой стромальный ответ (рис. 1).Шейка матки была интерпретирована как пораженная согласно внешнему отчету; однако было установлено, что это эндометриоз шейки матки. после просмотра. Следовательно, стадия IB была понижена. Ей было произведено иссечение мышечной массы поясничной мышцы, которое показало злокачественная опухоль оболочки периферических нервов (МПНСТ).
фигура 1(A&B) Вид с малым увеличением (20 ×) глубокой диффузной инфильтрации банальных желез (Случай 1). (C) Изображение в высоком увеличении (200 ×) обманчиво мягких желез эндометрия в глубоком миометрии. Строма эндометрия отсутствует (Случай 1). (D) Изображение с низким увеличением (20 ×) глубоко инвазивных желез эндометрия (20 ×) (Случай 2). (E) Инвазивные железы простираются на 0,3 см до серозной поверхности (20 ×) (Случай 2). (F) Изображение с высоким увеличением (200 ×) банальных желез эндометрия, проникающих в миометрий. Стромы эндометрия вокруг желез не видно (Случай 2).
Корпус 2
У 68-летней женщины с G5P5 было кровотечение в постменопаузе в течение 1 года. У нее сильная семейная история яичников и рак груди. Выскабливание эндометрия выявило сложную атипичную гиперплазию эндометрия. Пациент прошел тотальное гистерэктомия с двусторонней сальпингоофорэктомией.Поражения эндометрия практически не выявлено, и весь эндометрий был отправлен на гистологическую оценку. При микроскопическом исследовании поверхностный эндометрий показал сложную атипичную гиперплазию, но очаги мягких на вид желез эндометрия проникли глубоко в миометрий в нижнем сегменте матки / шейной области. Связанной стромы эндометрия вокруг этих желез не обнаружено. Эти железы прорастают до 77% толщины миометрия. (Фигура 1).Иммуноокрашивание проводилось для исключения эндоцервикальной аденокарциномы. Опухолевые клетки показали сильную ER- и PR-положительность, с пятнистым p16 и пятнистым окрашиванием виментином. Опухоль была классифицирована как pT2 (стадия II FIGO) из-за вовлечения стромы шейки матки.
Обсуждение
Диффузно инфильтративная или «злокачественная аденома-подобная» аденокарцинома эндометрия впервые была описана Митталом. и Барвик, в 1988 г. [1].В этом исследовании авторы описали 5 пациентов с 1 стадией заболевания. Два пациента умерли от болезни, и заключение было сделали, что хорошо дифференцированные аденокарциномы с «злокачественной аденомой» инвазии предвещают худший прогноз, чем обычный тип опухолевой инвазии. В 1994 году Ли и его коллеги описали два случая хорошо дифференцированной аденокарциномы. с аналогичным типом инвазии, с 1 рецидивом, а также пришли к выводу, что эти опухоли агрессивны [2].Однако в 1999 году Longacre и его коллеги сравнили две модели инвазии хорошо дифференцированных аденокарцином эндометрия; 50 случаев диффузно-инфильтративного типа с 50 случаями опухолей с обычным типом инвазии [3]. В большинстве случаев 92% случаев в группе с диффузным инфильтративным / аденомоподобным и 88% в группе с обычным типа инвазии были Стадия 1. Это исследование не обнаружило каких-либо существенных различий в безрецидивной выживаемости (RFS) среди две группы.Три пациента (3/50) с аденомно-злокачественной инвазией имели рецидив, и один пациент (1/50) в группе при обычном типе вторжения повторяется. Выживаемость также была одинаковой между двумя группами. Среднее время наблюдения в обеим группам было более 77 месяцев. Авторы пришли к выводу, что «аденомоподобный» тип инвазии миометрия не вызывает предвещают значительно худший прогноз, если контролировать стадию заболевания.Несоответствие между двумя исследованиями вероятно, из-за небольшого размера выборки в исследовании, проведенном Mittal et al. В 2002 году Май и его коллеги сообщили об аналогичном случае. без какой-либо дополнительной информации [4]. В 1995 году Нанбу и его коллеги описали 2 случая аденокарциномы шейки матки с минимальным отклонением от эндометриоидного типа. маточный сегмент; однако эти случаи считаются аденокарциномами злокачественной аденомы шейки матки после обзора статья [5].
Пациент 1 в этом отчете не имеет рецидивов или отдаленных метастазов через 9 лет после постановки диагноза, и мы считаем, что эти опухоли ведут себя аналогично обычным хорошо дифференцированным эндометриоидным карциномам эндометрия. Наличие МПНСТ у этого пациента. необъяснимо. Около половины MPNST связаны с синдромом нейрофиброматоза 1 (NF 1), и никаких известных ассоциаций не существует. между аденокарциномами эндометрия и МПНСТ.Пациент 1 не имел наследственных синдромов в анамнезе.
Диагностическое значение инвазии «злокачественной аденомы» заключается в наличии обманчиво мягких желез эндометрия.


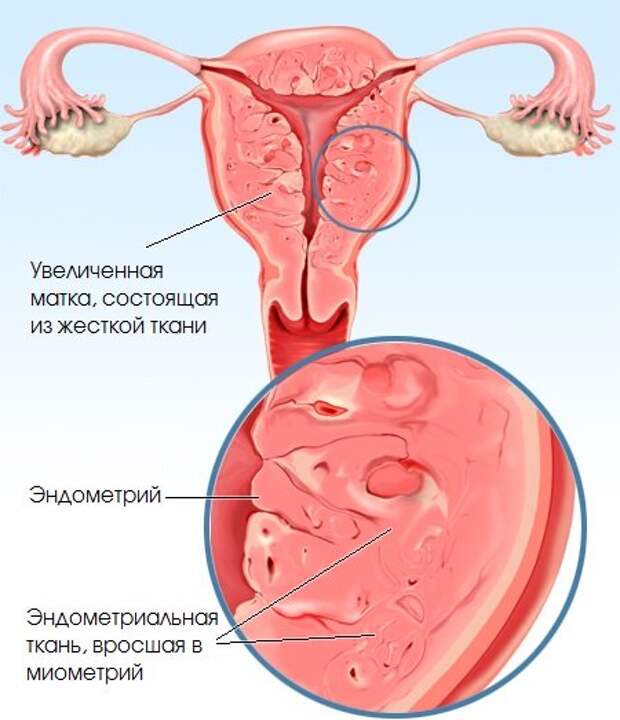 Разрезы матки, сделанные во время операции, такие как кесарево сечение (С-разрез), могут способствовать прямому вторжению клеток эндометрия в стенку матки.
Разрезы матки, сделанные во время операции, такие как кесарево сечение (С-разрез), могут способствовать прямому вторжению клеток эндометрия в стенку матки. Заболевание в такой форме не связано с гормональным фоном и нередко является предраковым состоянием, влекущим за собой образование злокачественной опухоли.
Заболевание в такой форме не связано с гормональным фоном и нередко является предраковым состоянием, влекущим за собой образование злокачественной опухоли.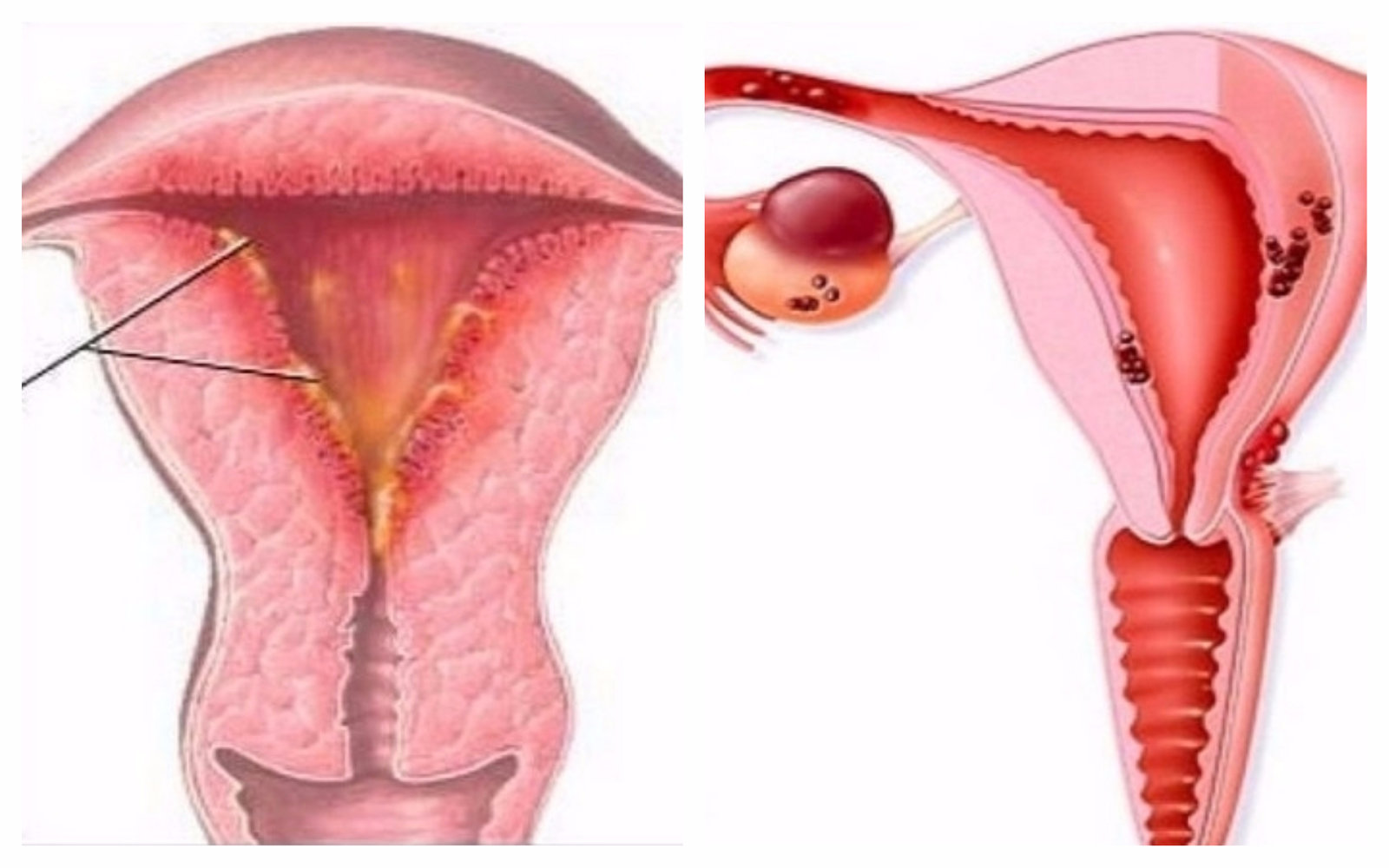 Назначается при железисто-кистовой гиперплазии эндометрия, а также при его толщине не более 16 мм.
Назначается при железисто-кистовой гиперплазии эндометрия, а также при его толщине не более 16 мм.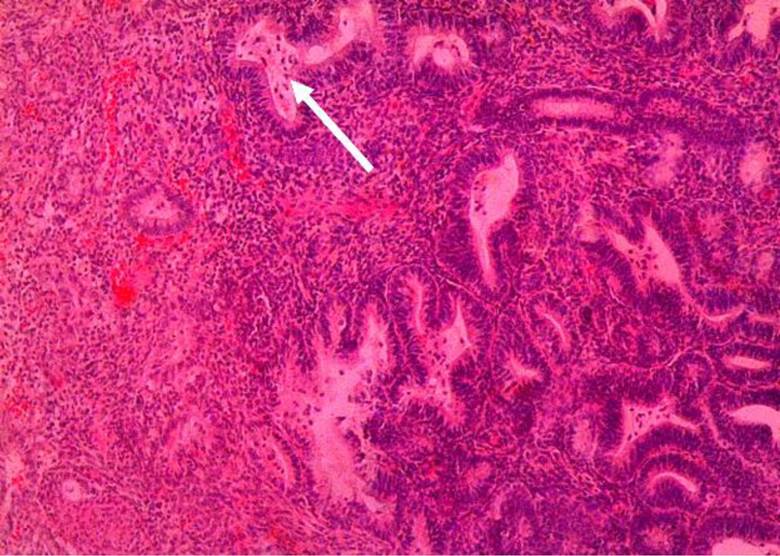
 Такой операции присущи многочисленные недостатки: сильные болевые ощущения, необходимость большого расширения шейки матки. риск возникновения спаечного процесса в малом тазу. Проводится под общим наркозом. Необходимость в госпитализации зависит от физического состояния пациента и способности переносить наркоз. Возможен местный наркоз обезболивающими препаратами.
Такой операции присущи многочисленные недостатки: сильные болевые ощущения, необходимость большого расширения шейки матки. риск возникновения спаечного процесса в малом тазу. Проводится под общим наркозом. Необходимость в госпитализации зависит от физического состояния пациента и способности переносить наркоз. Возможен местный наркоз обезболивающими препаратами.